Ammoniumnitraatti
| Rakenteellinen kaava | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
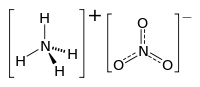
| ||||||||||||||||
| Yleistä | ||||||||||||||||
| Sukunimi | Ammoniumnitraatti | |||||||||||||||
| muut nimet |
|
|||||||||||||||
| Molekyylikaava | NH 4 NO 3 | |||||||||||||||
| Lyhyt kuvaus |
väritön kiinteä aine |
|||||||||||||||
| Ulkoiset tunnisteet / tietokannat | ||||||||||||||||
| ||||||||||||||||
| ominaisuudet | ||||||||||||||||
| Moolimassa | 80,04 g mol - 1 | |||||||||||||||
| Fyysinen tila |
kiinteä |
|||||||||||||||
| tiheys |
1,72 g cm −3 (20 ° C) |
|||||||||||||||
| Sulamispiste |
169 ° C |
|||||||||||||||
| kiehumispiste |
210 ° C (15 h Pa ), hajoaa 170 ° C: sta normaalipaineessa |
|||||||||||||||
| liukoisuus | ||||||||||||||||
| turvallisuusohjeet | ||||||||||||||||
| ||||||||||||||||
| Termodynaamiset ominaisuudet | ||||||||||||||||
| ΔH f 0 |
−366 kJ mol −1 |
|||||||||||||||
| SI -yksiköitä käytetään mahdollisuuksien mukaan ja tavanomaisesti . Ellei toisin mainita, annetut tiedot koskevat vakio -olosuhteita . | ||||||||||||||||
Ammoniumnitraatti on suola, joka muodostuu ammoniakista ja typpihaposta . Sitä käytetään erityisesti lannoitteiden ja räjähteiden valmistuksessa .
tarina
Ammoniumnitraattia tuotti ensimmäisen kerran vuonna 1659 Johann Rudolph Glauber saattamalla ammoniumkarbonaatin reagoimaan typpihapon kanssa. Vasta 1800 -luvun alussa Grindel ja Robin pitivät sitä korvikkeena kaliumnitraatille mustassa jauheessa käytettäväksi räjähteissä. Sen räjähdysominaisuudet raportoivat Reise ja Millon vuonna 1849, kun jauhemaisen ammoniumnitraatin ja hiilen seos räjähti kuumennettaessa. Tuolloin ammoniumnitraattia ei pidetty räjähteenä, vaikka pieniä tulipaloja ja räjähdyksiä ammoniumnitraatista on tapahtunut ympäri maailmaa. 1800 -luvun lopulla Euroopassa yritettiin rajoittaa mustan jauheen käyttöä hiilikaivoksissa ja löytää turvallinen korvike räjähteille. Englannissa, kun oli kokeiltu erilaisia räjähteitä, lopulta suositeltiin useita, joista suurin osa perustui ammoniumnitraattiin. Sekä dynamiitti että musta jauhe eivät läpäisseet testejä ja ne korvattiin ammoniumnitraattiin perustuvilla räjähteillä. Tämän komitean tulokset johtivat Britannian hiilikaivosasetukseen vuonna 1906. Vuoteen 1913 mennessä brittiläinen hiilen tuotanto saavutti kaikkien aikojen korkeimman tason, 287 miljoonaa tonnia, ja vuosittain käytettiin yli 5000 tonnia räjähteitä, joista vuodesta 1917 92% tästä määrästä perustui ammoniumnitraattiin. Räjähdysaineiden kustannusten alentamiseksi räjähteiden teollisuus lisäsi formulaatioihin enemmän halpaa ammoniumnitraattiyhdistettä, mutta sillä oli valitettava sivuvaikutus, joka lisäsi räjähteiden herkkyyttä kosteudelle. Kemistit voittivat tämän ongelman peittämällä ammoniumnitraatin erilaisilla epäorgaanisilla jauheilla, sekoittamalla sen dynamiittiin ja parantamalla räjähteiden pakkauksia veden pääsyn estämiseksi.
Päättymisen jälkeen ensimmäisen maailmansodan, joka on BASF kemian laitos vuonna Oppau tuotettu suuria määriä ammoniumnitraattia lannoitteena. Ammoniumnitraatin hygroskooppisten ominaisuuksien parantamiseksi , jotka ovat epäedullisia käytettäväksi lannoitteena , lisättiin aluksi kaliumkloridia , mikä johti muutokseen ammoniumkloridin ja kaliumnitraatin seokseksi, joka tunnettiin kaliumammoniumnitraattina. Kaliumkloridi korvattiin myöhemmin ammoniumsulfaatilla , jolloin syntyi tuote, joka tunnetaan nimellä ammoniumsulfaattinitraatti (kemiallisesti ammoniumsulfaattinitraatti ). Termiä Leuna -nitraatti, joka viittaa BASFin Leuna -tehtaaseen, käytetään joskus synonyyminä ammoniumsulfaattinitraatille. Oppaussa tuotettua ammoniumsulfaattinitraattia kutsuttiin usein yksinkertaisesti sekoitussuolaksi. Tämä tuote on sekä ensisijaisten (typpi) että toissijaisten (rikki) kasvien ravintoaineiden lähde. Kahden yhdisteen seos muodostaa joko vain näiden kahden yhdisteen seoksen tai kaksoissuolat (2AN-AS tai 3AN-AS) valmistusprosessista ja sekoitussuhteista riippuen. Kaksoissuolojen muodostuminen AN: sta ja AS: stä on ollut tiedossa vuodesta 1909 lähtien hollantilaisen fyysikon, kemian Franciscus AH Schreinemakersin (1864–1945) työstä. Aamulla 21. syyskuuta 1921 Oppaun tehtaalla tapahtui kaksi räjähdystä nopeasti peräkkäin , noin 400 tonnia ammoniumsulfaattinitraattia ja tappoi yli 500 ihmistä. Tämä räjähdys johti onnettomuuden laajoihin tutkimuksiin ja tutkimuksiin ammoniumsulfaattinitraatin mutta myös ammoniumnitraatin ominaisuuksista.
Toisen maailmansodan päättymisen jälkeen Yhdysvaltain hallitus alkoi toimittaa Eurooppaan lannoitelaatuista ammoniumnitraattia (FGAN), joka koostui rakeisesta ammoniumnitraatista, joka oli päällystetty noin 0,75% vahalla ja joka oli käsitelty noin 3,5% savella. Koska tätä materiaalia ei pidetty räjähteenä, sen käsittelyssä tai kuljetuksessa ei toteutettu erityisiä varotoimia - työntekijät jopa tupakoivat materiaalin lastaamisen aikana. Lukuisia kuljetuksia suoritettiin ilman vaikeuksia 16. ja 17. huhtikuuta 1947 saakka, kunnes tapahtui kauhea räjähdys. SS Grandchamp ja SS menestyjä, molemmat ankkuroitu Texas City Harbor ja täynnä FGAN, räjähti. Näiden katastrofien seurauksena Yhdysvalloissa käynnistettiin useita tutkimuksia räjähdysten mahdollisten syiden selvittämiseksi. Samalla tehtiin myös perusteellisempi tutkimus ammoniumnitraatin ja sen seosten orgaanisten ja epäorgaanisten materiaalien räjähdysominaisuuksista. Heti kun räjähdys tapahtui Texas Cityssä, vastaava räjähdys SS Ocean Libertyn aluksella järkytti Brestin satamaa Ranskassa 28. heinäkuuta 1947 . Tutkimukset osoittivat, että ammoniumnitraatti oli paljon vaarallisempaa kuin aiemmin luultiin, ja tiukemmat määräykset sen varastoinnista, lastaamisesta ja kuljetuksesta Yhdysvalloissa otettiin välittömästi käyttöön.
1970 -luvulla yhdysvaltalaiset yritykset Ireco ja DuPont alkoivat lisätä valmisteisiinsa alumiinia ja monometyyliamiininitraattia (MAN) geelimäisten räjähteiden valmistamiseksi, jotka voisivat räjähtää helpommin. Viimeaikainen kehitys koskee emulsioräjähteiden valmistusta (osittain ammonium- ja natriumnitraattiseosten kanssa ), jotka sisältävät ammoniumnitraattiliuoksen pisaroita öljyssä.
Valmistus
Ammoniumnitraattia (NH 4 NO 3 ) on muodostettu neutraloimalla ja ammoniakin kanssa typpihappoa .
Reaktio on voimakkaasti eksoterminen reaktiolämmöllä -146 kJ mol -1 .
ominaisuudet
Fyysiset ominaisuudet
Ammoniumnitraatti muodostaa värittömiä hygroskooppisia kiteitä, jotka sulavat 169,6 ° C: ssa. Kiinteä aine voi esiintyä viidessä eri polymorfisessa kiteisessä muodossa, siirtymälämpötilat -16,9 ° C, 32,3 ° C, 84,2 ° C ja 125,2 ° C. Kaksi ensimmäistä faasimuutosta lähellä huoneenlämpötilaa aiheuttavat ammoniumnitraattikiteiden taipumuksen tarttua yhteen. Polymorfiset muodot esiintyvät eri kidehilalla:
Muutosten kristallihila Polymorfi I 169,6 ° C ... 125,2 ° C kuutiometriä Polymorfi II 125,2 ° C ... 84,2 ° C nelikulmainen Polymorfi III 84,2 ° C ... 32,2 ° C ortorombinen Polymorfi IV 32,2 ° C ... -16,9 ° C ortorombinen Polymorfi V <-16,9 ° C nelikulmainen
Vaiheiden siirtyminen polymorfien IV ja III välillä 32,2 ° C: ssa on olennaista käsiteltäessä, mutta myös aineen varastoinnin aikana. Lannoitteiden tai räjähteiden valmisteissa tämä käyttäytyminen voi johtaa ei -toivottuihin muutoksiin morfologiassa ja siten ominaisuuksissa. Tämä vaihesiirto voidaan estää seostamalla eri suoloilla niin kutsutun faasistabiloidun ammoniumnitraatin saamiseksi. Sopivia suoloja voivat olla erilaiset kaliumsuolat, kuten kaliumfluoridi , kaliumkloridi , kaliumnitraatti , kaliumkarbonaatti , kaliumsulfaatti , kaliumrodanidi ja kaliumdikromaatti , joita on kuitenkin lisättävä suhteessa 1 - 2 painoprosenttia ( massaprosenttia). Vaikutus voidaan saavuttaa myös, jossa on huomattavasti pienempi määrä 0,1 paino-% kaliumia hexacyanidoferrate (II) K 4 [Fe (CN) 6 ] .3H 2 O.
Ammoniumnitraatin hygroskooppisella luonteella on vahva sulamispisteen alentaminen : Jopa vain 1 % : n veden imeytyminen alentaa suolan sulamispistettä noin 156 ° C: ssa. Sitä vastoin vaihekaavio esittää eutektikan , jonka sulamispiste on -16,9 ° C ja ammoniumnitraattipitoisuus on 42 painoprosenttia. - Ammoniumnitraatti, joka liukenee hyvin helposti veteen, alentaa veden sulamispistettä jopa 42 painoprosenttiin, jolloin sitä käytetään mm. perustuu kylmiin seoksiin . Suuremmilla massaosuuksilla ammoniumnitraattia on läsnä kahdessa vaiheessa, toisaalta vesiliuos, toisaalta itse suola kiinteänä sedimenttinä (20 ° C: ssa noin 65 painoprosentista , 100 ° C: ssa noin 91,5 painoprosenttia ):
Korkeassa paineessa vesiliukoisuus laskee rajusti: Normaalipaineessa ja 25 ° C: ssa seos sisältää edelleen 67,6 painoprosenttia ammoniumnitraattia, 12 kbar: n paineeseen asti tämä osuus laskee vain 25,4 painoprosenttiin. Kun paine on 12,1 kbar ja pitoisuus 25,3 painoprosenttia, faasien rajaviivat leikkaavat yksivaiheisen liuoksen ja liuoksen ja jään tai liuoksen ja ammoniumnitraatin kaksivaiheisen seoksen välillä polymorfina IV. Tämän paineen yläpuolella on jään ja kiinteän ammoniumnitraatin kaksivaiheinen seos, eikä liuosta voi enää olla olemassa.
Puhtaan ammoniumnitraatin tiheys on 1,725 g · cm −3 . Vesiliuoksessa tiheys kasvaa pitoisuuden kasvaessa ja pienenee lämpötilan noustessa.
Ammoniumnitraatin vesiliuoksen tiheys eri lämpötiloissa Palkka (Ma%) 20% 30% 40% 50% 60% 70% 80% 90% 94% 20 ° C 1.0830 1,1275 1,1750 1,2250 1,2785 40 ° C 1,0725 1.1160 1.1630 1.2130 1,2660 1.3220 60 ° C 1.0620 1.1045 1.1510 1.2005 1,2525 1.3090 1,3685 80 ° C 1,0550 1,0935 1.1390 1,1875 1.2395 1.2960 1,3550 100 ° C 1.0410 1.0820 1.1270 1.1745 1,2265 1,2825 1,3420 1,4075 120 ° C 1,3285 1,3930 1.4210 140 ° C 1,3785 1,4065 160 ° C 1,3940
In metanolia , tuloksena on 20% liuos 30 ° C: ssa ja 40%: ista liuosta 60 ° C: ssa Liukoisuus etanoliin on paljon pienempi. Täällä voidaan saada vain 4% liuos 20 ° C: ssa.
Kemiallisia ominaisuuksia
Kuumennettaessa (T> 170 ° C) ammoniumnitraatti hajoaa yhtälön mukaisesti
on veteen ja typpioksiduulin . Vahvan alkukipinän vuoksi se hajoaa seuraavasti:
Typpiatomi nitraatti-ioni NO 3 - ( hapetus taso + V) hapettaa typpiatomin ammoniumioni NH 4 + (hapetus taso-III), niin että lopulta, että N- 2 -molekyyli, molemmat typpiatomit ovat samalla hapetustasolla (tässä 0). Tällaisia reaktioita, joissa atomit hapettavat saman alkuaineen muita atomeja ja jotka itse pelkistyvät siten, että lopulta kaikki ovat samalla hapetustasolla, kutsutaan sopiviksi .
Tämän reaktion räjähtävä siirtyminen kiinteästä aineesta (NH 4 NO 3 ) yksinomaan kaasumaisiin tuotteisiin (H 2 O, N 2 ja O 2 ) selittää ammoniumnitraatin suuren räjähdysvoiman : Noin 980 l / kg sillä on yksi suurimmat ominaishöyrytilavuudet ja Jos otat huomioon myös sen tiheyden, suhde on vielä suurempi (höyrytilavuus / räjähtävä tilavuus). Muita tärkeitä räjähdysilmaisimia ovat:
- Räjähdyslämpö : 2625 kJ kg −1
- Räjähdysnopeus : 2500 m · s −1 tiheydellä 1,4 g · cm −3
- Lyijylohkon laajennus : 180 cm 3 / 10g
- Iskun herkkyys : 49 Nm
- Kitkaherkkyys : Ei reaktiota 353 N tapin kuormitukseen asti
- Teräsholkkitesti : rajahalkaisija 1,0 mm
Reagoimalla väkevän rikkihapon kanssa ja sen jälkeen tislaamalla voidaan saada talteen typpihappo , joka on lähtöaine monien räjähteiden valmistuksessa:
käyttää
Ammoniumnitraatti on monien lannoitteiden pääkomponentti ( ammoniumnitraatti-urea-liuos , monimutkainen lannoite ("sininen rake "), kalsium-ammoniumnitraatti (Nitramoncal, Chemie Linzin tuotenimi, sisäinen NAC )).
Sitä käytetään myös räjähteisiin . Ammoniumnitraattia on esimerkiksi hajotusaineissa ANC , Donarit ja Kinepak .
Ammoniumnitraattia käytettiin ajoittain myös moottoriajoneuvojen turvatyynyjen ponneaineena . Se osoittautui kuitenkin riittämättömän pitkäaikaiseksi vakaaksi erityisesti korkean ympäristön lämpötilan ja kosteuden vaikutuksesta, ja se korvattiin muilla paisutteilla. Pelkästään Yhdysvalloissa yli 40 miljoonaa ajoneuvoa oli palautettava, koska ainakin yhdessä turvatyynyssä oli ammoniumnitraattia sisältävä kaasugeneraattori.
Vaikka sitä pidetään hapettava ja voi räjähtää, kun sitä kuumennetaan, ammoniumnitraatti ei ole yksi todella räjähtäviä aineita tarkoitettu, että räjähteiden lain . Siitä huolimatta sen käyttöä Saksan liittotasavallassa säännellään räjähdelailla, joten ammoniumnitraattia saa käyttää vain lannoitteissa, joihin on sekoitettu vaarattomia aineita, kuten kalkkia (KAS27) sen mahdollisen vaaran vuoksi. Valmistajan Chemie Linzin tyypilliset pitoisuudet olivat aiemmin 26 ja 28% N (typpipitoisuus). Nykyään 27% N on yleistä, mikä tarkoittaa noin 70% NH 4 NO 3: a ja loput kalkkia ja vähän öljyä, jotta pallot eivät tartu yhteen. Urealla voidaan saavuttaa korkeampi, jopa 46% typpipitoisuus , sen amidityppi on saatavilla hitaammin.
Vaarallisuutensa vuoksi EU on laskenut ammoniumnitraatin, jonka typpipitoisuus suhteessa ammoniumnitraattiin on yli 16%, yhdeksi räjähteiden rajoitetuista lähtöaineista 1. helmikuuta 2021 lähtien , minkä seurauksena toimitukset, käyttö, hallussapito ja ihmisten siirtäminen on kielletty, jos he eivät ole aktiivisia ammatillisiin tai kaupallisiin tarkoituksiin; Ammattimainen tai kaupallinen tarkoitus on tarkastettava myynnin yhteydessä, ja epäilyttävistä tapahtumista ja varkauksista on ilmoitettava. 27. kesäkuuta 2010 (siirtymäsäännökset 1.7.2014 asti) seosten, joiden typpipitoisuus on yli 16%, markkinoille saattaminen on kielletty EU: ssa, paitsi maanviljelijöitä ja vastaavia kaupallisia käyttäjiä.
Katastrofit
Ammoniumnitraatti on syy lukuisiin räjähdyskatastrofeihin :
- Räjähdys ammoniakin kasvi on BASF: in Oppau (nyt piirin Ludwigshafen Rein ) 21. syyskuuta 1921: jähmettynyt ammoniumsulfaattinitraatti- -Dünger oli siellä yleensä ilmattu ennen poistovälineet dynamiittia. Tuotantoprosessin muutoksen vuoksi tuotteessa oli todennäköisesti paikallista ammoniumnitraatin kertymistä. Räjähdykset aiheuttivat kaksi räjähdystä nopeasti peräkkäin, jolloin noin 400 yhteensä 4500 tonnista lannoitetta räjähti siilossa aiheuttaen yhden historian suurimmista vahingoista: 559 ihmistä kuoli, loukkaantui vuonna 1977 ja suuri osa tehtaasta ja ympäröivä alue Rakennukset tuhoutuivat. Räjähdys kuultiin jopa 300 kilometrin päässä olevaan Müncheniin.
- Vuonna Texas City räjähdys 16. huhtikuuta 1947 kaksi rahtilaivat Grandcamp ( Ranska ) ja eteenpäin pyrkivä henkilö (USA) täynnä n. 2300 tonnia ammoniumnitraattia räjähti satamassa Texas City on Yhdysvalloissa . Kuolleita oli 500–600, yli 100 kadonneita, 8000 loukkaantunutta, satoja kodittomia ja 65 miljoonan dollarin vahingot.
- 28. heinäkuuta 1947 ammoniumnitraatilla lastattu rahtialus Ocean Liberty ( Norja ) räjähti Brestin satamassa (Ranska ). Kuolleita oli 26 ja loukkaantuneita yli 100.
- Saapui 9. tammikuuta 1963 Ouluun ( Suomi ) räjähdykseen typpitehtaassa, kuoli, kun 10 työntekijää.
- Vuonna 19 huhtikuu 1995 pommitus Murrah liittovaltion rakennuksen Oklahoma City Yhdysvalloissa, oikeistolainen terrori Timothy McVeigh murhasivat 168 ihmistä, joista 19 lapsia päiväkodissa, ja loukkaantui yli 800 toiset lyömällä yksi hänen autopommien itse tehty, 2,4 tonnin ammoniumnitraatista ja nitrometaanista valmistettu räjähdysaine räjähti, mikä aiheutti kahdeksankerroksisen hallintorakennuksen romahtamisen. Yli 300 muuta rakennusta vaurioitui.
- Täsmälleen 80 vuotta Oppaun ammoniakkitehtaan räjähdyksen jälkeen (ks. Yllä) 31 ihmistä kuoli 21. syyskuuta 2001 ammoniumnitraattiräjähdyksessä AZF -lannoitetehtaassa Toulousessa, Ranskassa. Lisäksi sattui tuhansia loukkaantumisia ja valtavia omaisuusvahinkoja.
- Vuonna Ryongchon junaonnettomuus 22. huhtikuuta 2004 junanvaunuksi ladattu ammoniumnitraatin räjähti vuonna Ryongchon , Pohjois-Koreassa, tappaen ainakin 161 ihmistä. Arviolta 1300 ihmistä loukkaantui ja 8000 kotia tuhoutui tai vaurioitui.
- 22. heinäkuuta 2011, äärioikeistolaisen salamurhaaja Anders Behring Breivik räjäytti autopommi perustuva 950 kiloa ANFOa (ammoniumnitraatin ja dieselöljy ) on Oslon hallituksen piirissä Norjassa osana hänen sarjassa hyökkäyksiä . 8 ihmistä kuoli, 10 loukkaantui.
- Ainakin 14 ihmistä kuoli ja 180 loukkaantui tulipalossa ja väkivaltaisessa räjähdyksessä West Fertilizer Companyn tehtaalla Texasissa 17. huhtikuuta 2013.
- 12. elokuuta 2015 satoja ihmisiä kuoli tai loukkaantui räjähdyksessä Tianjinissa Kiinassa . Brittiläisen The Guardian -lehden mukaan paikalla varastoitiin 800 tonnia ammoniumnitraattia ja lukuisia muita aineita. Tämä määrä on sopiva selittämään räjähdyksen jättämän noin 100 m leveän kraatterin. Ei tiedetä, mikä aine aiheutti suurimman osan tuhosta.
- 4. elokuuta 2020 Libanonin pääministerin mukaan 2750 tonnin ammoniumnitraatin valtava räjähdys tuhosi Beirutin sataman ja suuren osan ympäröivästä alueesta. Räjähdys kuultiin satojen kilometrien päästä.
Katso myös
Yksilöllisiä todisteita
- ↑ Merkintä AMMONIUMNITRAATTI vuonna CosIng tietokantaan EU: n komission, pääsee 28. joulukuuta 2020 mennessä.
- ↑ b c d e f Merkintä ammoniumnitraatin on GESTIS aine tietokanta IFA , pääsee 10. tammikuuta, 2017 mennessä. (JavaScript vaaditaan)
- ↑ a b c L. H. Adams, RE Gibson: Tasapaino binaarijärjestelmissä paineen alla. III. Paineen vaikutus ammoniumnitraatin liukoisuuteen veteen 25 °: ssa . Julkaisussa: J. Am. Chem. Soc. nauha 54 , ei. 12 , 1932, s. 4520–4537 , doi : 10.1021 / ja01351a008 .
- ↑ a b c d e f g h i j k l Karl-Heinz Zapp, Karl-Heinz Wostbrock, Manfred Schäfer, Kimihiko Sato, Herbert Seiter, Werner Zwick, Ruthild Creutziger, Herbert Head: Ammonium Compounds . Julkaisussa: Ullmann's Encyclopedia of Industrial Chemistry . Wiley-VCH, Weinheim 2005, ISBN 978-3-527-30673-2 , Ammoniumyhdisteet, doi : 10.1002 / 14356007.a02_243 .
- ↑ Dimetyylisulfoksidin (DMSO) liukoisuustiedot . Julkaisussa: Gaylord Chemical Company, LLC (toim.): Tiedote 102 . Kesäkuuta 2014, s. 15 ( gaylordchemical.com [PDF; käytetty 6. elokuuta 2020]).
- ↑ Frank-Michael Becker ja muut: Kaavakokoelma . 3. Painos. Paetec, Berliini 2003, ISBN 3-89818-700-4 , s. 116 .
- ^ Vaclav Smil: Kahdenkymmenennen vuosisadan luominen: Tekniset innovaatiot 1867-1914 ja niiden kestävä vaikutus . Oxford University Press, 2005, ISBN 978-0-19-803774-3 , s. 185 ( books.google.de ).
- ^ A b c Jacqueline Akhavan: Räjähteiden kemia . Royal Society of Chemistry, 2011, ISBN 978-1-84973-330-4 , s. 5 ( rajoitettu esikatselu Google -teoshaussa).
- ↑ Tor E. Kristensen: Tosiseikkojen selvennys ja kemikaalitekninen uudelleenarviointi vuoden 1921 Oppaun räjähdysonnettomuudesta huokoisen ammoniumsulfaattinitraattilannoitteen odottamattoman räjähtävyyden suhteen. (PDF; 1,6 Mt) 16/01508. Julkaisussa: FFI-RAPPORT. Norwegian Defense Research Establishment / Forsvarets forskningsinstitutt, 4. lokakuuta 2016, s. 20 , luettu 1. tammikuuta 2020 .
- ↑ George Stanley Scott, RL -apuraha: Ammoniumnitraatti - sen ominaisuudet sekä palo- ja räjähdysvaarat . Yhdysvaltain sisäministeriö, Bureau of Mines, 1948, s. 23 ( rajoitettu esikatselu Google -teoshaussa).
- ↑ a b c d Rudolf Meyer, Josef Köhler, Axel Homburg, Rudolf Meyer, Axel Homburg,: Explosivstoffe . 10., täysin tarkistettu. Painos. Wiley-VCH, Weinheim 2008, ISBN 978-3-527-62341-9 .
- ↑ C.Oommen, SR Jain: Ammoniumnitraatin vaihemuutos kaliumsuoloilla . Julkaisussa: Journal of Thermal Analysis and Calorimetry . nauha 55 , ei. 3 , 1999, s. 903-918 , doi : 10.1023 / A: 1010146203523 .
- ↑ Anuj A.Vargeese, Satyawati S.Joshi, VN Krishnamurthy: Kaliumferrosyanidin käyttö tavanomaisena modifikaattorina ammoniumnitraattikiteiden koon pienentämisessä ja faasimuutoksissa lietteissä . Julkaisussa: Journal of Hazardous Materials . nauha 180 , ei. 1 , 2010, s. 583-589 , doi : 10,1016 / j.jhazmat.2010.04.073 .
- ↑ Anuj A. Vargeese, Krishnamurthi Muralidharan, VN Krishnamurthy: lämmönkestävyys tapa muutettu ammoniumnitraatin: Havaintoja isoconversional kineettinen analyysi . Julkaisussa: Thermochimica Acta . nauha 524 , ei. 1 , 2011, s. 165–169 , doi : 10.1016 / j.tca.2011.07.009 .
- ↑ Bernd Engels, Reinhold Fink, Tanja Schirmeister , Carsten Schmuck : Kemia lääketieteen ammattilaisille . 1. painos. Addison-Wesley julkaisussa Pearson Education Germany, München 2008, ISBN 978-3-8273-7286-4 .
- ^ AF Holleman , E. Wiberg , N. Wiberg : Epäorgaanisen kemian oppikirja . 101 painos. Walter de Gruyter, Berliini 1995, ISBN 3-11-012641-9 , s.65 .
- ↑ Neil Gough, Jonathan Soble, Hiroko Tabuchi: Viallinen Takata -turvatyyny kasvaa maailmanlaajuiseksi ongelmaksi valmistajalle. Julkaisussa: New York Times verkossa. 18. marraskuuta 2014, käytetty 14. huhtikuuta 2019 .
- ↑ Takata Airbag Recall: Kaikki mitä sinun tarvitsee tietää. Julkaisussa: Consumer Reports. 29. maaliskuuta 2013, käytetty 16. huhtikuuta 2019 .
- ↑ Art. 5 Asetuksen (EU) 2019/1148 Euroopan parlamentin ja neuvoston 20. kesäkuuta 2019 markkinoille saattamista ja käyttöä esiasteiden räjähteiden liitteen I voimaantulon Art. 23, tutkimus ja raportointivelvoitteet taloudellisen operaattoreille ja online -kauppapaikoille 8 ja 9. Saksassa hallussapito-, käyttö-, siirto- ja myyntikiellon rikkomisesta rangaistaan raaka -ainelain 13 §: n mukaan
- ↑ Asetuksen (EY) N: o 1906/2006 67 artikla ja liitteen XVII kohta 58.
- ^ Hans Schuh :: Toulousen arvoitus . Julkaisussa: The time . Ei. 41 , 2001, s. 39 ( zeit.de - Katsaus ammoniumnitraattikatastrofeihin.)
- ^ Christian Haller: BASFin räjähdysonnettomuus 21. syyskuuta 1921. Katastrofien havaitseminen ja käsittely lehdistössä, politiikassa ja asiantuntijoissa . Julkaisussa: Lehti Ylä -Reinin historiasta . Ei. 161 , 2013, s. 327-328 .
- ↑ RM Goody: Stratosfäärin fysiikka . Cambridge University Press, 2014, ISBN 978-1-107-69606-8 , s. 32 ( koko teksti Googlen teoshaussa).
- ^ Jälki. ( Muisto 26. marraskuuta 2015 Internet -arkistossa ) julkaisussa: The 1947 Texas City Disaster. Moore Memorial Public Library, 2. huhtikuuta 2007.
- ↑ Emina Mamaca et ai.: Review of Chemical Spills at Sea and Lessons Learned. 2009, s. 17 (Interspill Conference of the Center of Documentation, Research and Experimentation on Accidental Water Pollution ).
- ↑ Sébastien Panou: 28. heinäkuuta 1947, l'Ocean Liberty räjähtää. Lähde : maville.com. brest.maville.com, 28. heinäkuuta 2007, käytetty 6. elokuuta 2020 (ranska).
- ↑ Kohtalokkaasta tehdasräjähdyksestä 55 vuotta - koko Oulun kaupunki vavahteli ja uhreja on vieläkin kateissa. Haettu 8. elokuuta 2020 (suomi).
- ↑ Kun Typpi räjähti, koko Oulu heräsi - oululaisten mieleen syöpyneen Typpi Oy: n räjähdyksen muuttaminen sama ammoniumnitraatti kuin Beirutin räjähdyksen. Haettu 8. elokuuta 2020 (suomi).
- ↑ Tappava Texas -räjähdys "kuin tornado" . Julkaisussa: BBC News . BBC News , 18. huhtikuuta 2013 ( bbc.com ).
- ↑ Lannoitelaitos Texasissa: Räjähdys jättää kuvan tuhoista. Julkaisussa: orf.at. news.ORF.at , 13. huhtikuuta 2013, käytetty 6. elokuuta 2020 .
- ^ Fergus Ryan: Tianjinin räjähdykset: varasto "käsitteli myrkyllisiä kemikaaleja ilman lupaa" - raportoi . Julkaisussa: The Guardian . 2015 ( theguardian.com ).
- ↑ Beirut: Mistä vaarallinen ammoniumnitraatti tulee? Julkaisussa: tagesschau.de. Haettu 6. elokuuta 2020 .
kirjallisuus
- Vaarallisten aineiden komitea (toim.): Tekninen sääntö vaarallisille aineille. TRGS 511 ammoniumnitraatti . (PDF; 431 kt). Marraskuuta 2008
- Richard Escales: Ammoniittiset typpiräjähteet . Books on Demand, Norderstedt 2002, ISBN 3-8311-3563-0 (uusintapainos 1909 painoksesta)
- Erica Lotspeich, Vilem Petr: The Characterization of Ammonium Nitrate MiniPrills , Luku 45, Materiaalien dynaaminen käyttäytyminen, Volume 1: Proceedings of the 2014 Annual Conference on Experimental and Applied Mechanics, Springer, 2014, sivut 319 ja sitä seuraavat kohdat ( Googlebooks )
- K. Hahnefeld, R. Gill, G. Buske: Vaikuttaa ammoniumnitraatin räjähdyskykyyn . Wirtschaftsverlag NW, Bremerhaven 1983, ISBN 3-88314-308-1
- W. Pittman, Zhe Han, B.Harding, C.Rosas, Jiaojun Jiang, A.Pineda, MS Mannan: Oppiaiheita ammoniumnitraattikatastrofien analyysistä viimeisten 100 vuoden aikana . Julkaisussa: J. Hazard. Mat. 280, 2014, s. 472-477, doi: 10.1016 / j.jhazmat.2014.08.037










