Alkynes
Alkyynit (aiemmin asetyleenit ja asetyleenihiilivedyt ) ovat kemiallisia yhdisteitä alifaattisten hiilivetyjen ryhmästä, joilla on molekyylissä vähintään yksi hiili-hiili-kolmoissidos (R-C = C-R). Alkyynien vain yksi tällainen kolmoissidoksen muodostavat homologisen sarjan kanssa yleisen empiirinen kaava C n H 2 n- -2 (jossa n = 2, 3, 4, ...), joka alkaa kanssa etyynistä .
Yhdisteitä, joissa on kaksi tai useampia hiili-hiili-kolmoissidoksia, kutsutaan polyyneiksi ; laajemmassa mielessä asykliset hiilivedyt, joissa on useita hiili-hiili-kolmoissidoksia, voidaan laskea alkyynien joukkoon.
Sykliset yhdisteet, joissa on hiili-hiili-kolmoissidos, lasketaan toisaalta sykloalkyyneihin ja aromaattisia hiilivetyjä, joilla on muodollinen kolmoissidos renkaassa, kutsutaan aryyneiksi .
historia
Ensimmäistä kertaa asetyleeni (etyni), yksinkertaisin alkyyni, saatiin vuonna 1836 Edmund Davylta , Royal Dublin Societyn kemiaprofessorilta ja kuuluisan englantilaisen kemisti Humphry Davyn serkulta . Yrittäessään edustaa kaliumia metallimuodossa, hän sai etyniä kuumentamalla kaliumsuoloja, kuten kaliumasetaattia tai kaliumkarbonaattia , hiilellä , mitä seurasi muodostuneen kaliumkarbidin reaktio veden kanssa. Löytö kuitenkin unohdettiin. Vuonna 1862 saksalainen kemisti ja lääkäri Friedrich Wöhler onnistui valmistamaan asetyleeniä saattamalla vesi reagoimaan kalsiumkarbidin kanssa . Vuonna 1863 ranskalainen kemisti Marcelin Berthelot onnistui kuvaamaan elementit käyttämällä grafiittielektrodien välistä valokaarta vetyatmosfäärissä. Hän nimesi kaasuasetyleenin. Vuonna 1895 Henry Le Chatelier huomasi, että asetyleeni palaa hapella erittäin kuumalla liekillä. Tämä loi perustan asetyleenihitsaukselle ja leikkaukselle.
Homologinen sarja
Tässä ovat tärkeimmät alkyynien päässä etyyni (C 2 H 2 ) (asetyleeni) ja dekyyni (C 10 H 18 ), niiden nimet ja empiirinen kaava:
- Etyyni : C 2 H 2
- Propyyniä : C 3 H 4
- 1-butyyni : C 4 H 6
- 2-butyyni : C 4 H 6
- Pentyyni : C 5 H 8
- Heksyyni : C 6 H 10
- Heptyynin : C 7 H 12
- Oktaniini : C 8 H 14
- Nonin : C 9 H 16
- Decin : C 10 H 18
nimikkeistö
Alkyynien nimeäminen IUPAC- sääntöjen mukaan perustuu alkaanien nimiin . Alkyynin varren nimi valitaan alkaanin juurisanasta, jolla on sama määrä hiiliatomeja, ja loppuliite -an korvataan -in: llä . Haaroittuneiden alkyynien tapauksessa pisin mahdollinen hiiliketju, jossa on kolmoissidos, antaa varren nimen. Alkyneillä on korkeampi prioriteetti kuin alkeeneilla. Kaksi ensimmäistä edustajat homologisen sarjan tämän ryhmän aineet ovat etyyni (H - C = C - H) ja propyyni (H - C = C - CH 3 ). Kolmoissidoksen sijainti on kuvattu numerolla sen edessä niin, että se on mahdollisimman pieni, esim. B. 1-butyyni (H-C = C-CH 2 -CH 3 ) ja 2-butyyni (H 3 C-C = C-CH 3 ). Jos hiiliketju sisältää useita kolmoissidoksia, siihen lisätään di , tri- , tetra- jne. Edessä tavu on nimi . Alkyyni, jossa on viisi (Kreikka penta ) hiiliatomia ja kaksi kolmoissidosta jälkeen 1. ja 4. hiiliatomin annetaan IUPAC-nimi 1,4-pentadiyne (H - C = C - CH 2 -C = C - H). Rakenteelliset isomeeriset 1,3-pentadiyne on seuraava rakenne: H - C = C - C = C - CH 3 .
Sähköinen rakenne
Alkyynien kolmoissidos koostuu sp-hybridisidoksesta ja kahdesta ortogonaalisesta p-sidoksesta. Nämä kaksi ortogonaalista p-sidosta (ortonormaalinen perusta) muodostavat kaksi kiertymätöntä orbitaalia, jotka z. B. voidaan havaita IR-spektroskooppiset tutkimukset W 2 (CO) 6 . Johtuen s-orbitaalien suuremmasta osuudesta sp-hybriditiebitaaleissa, todennäköisyys, että CH-sidoselektronit sijaitsevat lähellä hiiliatumia, on suurempi kuin alkeenien (sp 2 ) ja alkaanien (sp 3 ) kohdalla, jolloin CH-happamuus on terminaalisempi (terminaali) alkyynejä. Siksi s K S arvo on ethine 25 on huomattavasti pienempi kuin eteenin (44) tai etaania (50). Vahvoilla emäksillä terminaalinen hiiliatomi voidaan deprotonoida alemmissa alkyyneissä ja z. B. korvataan metalliatomilla. Alkyynien suoloja kutsutaan asetylideiksi . Lyhennetystä CH-sidoksesta johtuvan heikon CH-polaarisuuden lisäksi alkyylit ovat suhteellisen polaarisia. C3C-kolmoissidoksen elektronisesta rakenteesta seuraa, että kolmoissidoksen C-atomit ja nämä kahteen suoraan atomiin liitetyt atomit ovat linjassa linjassa (lineaarinen). Kolmoissidoksen hiili-hiili-etäisyys on 120 pm ja on siten lyhyempi kuin C = C-kaksoissidoksen etäisyys.
Spektroskooppiset ominaisuudet
1 H-NMR
In 1 H-NMR , alkynyyli vetyatomit eivät ole niin vahvasti deshielded kuin alkenyyli vetyatomia, koska pyörähdyssymmetrinen kolmoissidos ulkoinen magneettikenttä indusoi renkaan virta, jonka magneettikenttä on vastapäätä ulkoisia. Koska kolmoissidos välittää spin-spin-kytkennän hyvin, 4 J-kytkimellä neljän sidoksen yli ja 5 J-kytkimellä yli viiden sidoksen kytkentävakiot ovat yleensä 1-3 Hz. Etäkytkennässä tämä on suhteellisen suuri arvo, joten se on usein ominaista alkynyyliryhmälle .
Infrapunaspektroskopia
On lisäksi 13 C-NMR-spektroskopialla, infrapuna- spektroskopia on käyttökelpoinen menetelmä tunnistaa päätelaitteen alkyyni, kuten voimakas tunnusomainen kaistan CC venytys värähtely on esitetty noin 2100 cm -1 .
Uutto ja etiinin valmistus
- Kalsiumkarbidin uuttaminen ja sitä seuraava hydrolyysi
- Kalsiumoksidi ja koksi reagoivat muodostaen kalsiumkarbidia ja hiilimonoksidia .
- Kalsiumkarbidi ja vesi reagoivat muodostaen etyniä ja kalsiumhydroksidia .
- Metaanin dimerointi ja dehydraus
- Tietyissä olosuhteissa metaani reagoi muodostaen etiiniä ja vetyä.
- Osittainen metaanihapetus
- Metaani hapettuu eteeniksi, hiilimonoksidiksi ja vedyksi.
Reaktiot
Hydraus
Hydraus normaalilla katalyytillä
Alkyynit voidaan hydraa vedyllä alkaaneiksi tavallisten katalyyttien, kuten platinan tai palladiumin, avulla.
Hydraus myrkytetyllä katalyytillä
Myrkytetyllä katalyytillä, Lindlar-katalysaattorilla , alkyni reagoi vain alkeenin muodostamiseksi. Vain ( Z ) -alkeeneja ( cis ) muodostuu, koska vetyatomit lähestyvät alkyniä samalla puolella ja reagoivat.
Alkynyylidien muodostuminen
Koska terminaaliset alkyynit, kuten jo mainittiin, ovat CH-happoja, ne voivat reagoida niin kutsuttujen alkynyylidien muodostamiseksi. Nestemäisessä ammoniakissa olevien alkalimetallien kanssa ne muodostavat alkalialkyylididejä. Liukenemattomat raskasmetallialkynyylididit muodostuvat hopea (I) - ja kupari (I)-suolojen vesiliuoksiin. Kuivina nämä ovat kuitenkin erittäin räjähtäviä!
Elektrofiilinen lisäys
Lisäys kolmoissidokseen on eksotermisempi kuin kaksoissidoksen lisääminen.
Alkyynit ovat kuitenkin vähemmän reaktiivisia kuin alkeenit elektrofiilisiä reagensseja kohtaan. Ilmeinen ristiriita voidaan selittää välituotteiden karbeniumkationien stabiilisuudella:
Alkyylikationi on paljon vakaampi kuin vinyylikationi, joten elektrofiilien lisäysreaktio alkyyneihin estetään kineettisesti (= suurempi aktivaatioenergia).
Halogenointi
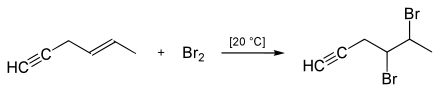
Hallabin menetelmän mukaan halogenointi tapahtuu seuraavasti: CC-kolmoissidos on vähemmän nukleofiilinen kuin hiili-hiili-kaksoissidos, minkä vuoksi halogeenit eivät lisää spontaanisti kolmoissidosta. Tämä tapahtuu vain silloin, kun halogeeni-sidos on polarisoitu avulla Lewis-hapon, esimerkiksi FeCI 3 tai AICI 3 . Tämä tuottaa ( E ) -1,2-dihaloalkeenia stereoselektiivisesti .
Siksi hiili-hiili-kolmoissidoksen läsnä ollessa hiili-hiili-kaksoissidos voidaan halogenoida selektiivisesti niin kauan kuin Lewis-happoa ei lisätä.
Hydrohalogenointi
Vetyhalogenidia voidaan lisätä alkyyneihin ensimmäisessä vaiheessa, jolloin saadaan vinyylialogeeninen halogeenialkeeni. Nämä reagoivat kuitenkin edelleen muodostaen dihalogeeneja voimakkaammissa olosuhteissa, koska ne eivät ole kovin reaktiivisia. Mukaan Markovnikoff sääntö, 1,1-dihaloalkaanit muodostuvat täällä.
Etyylin hydrokloorilla vinyylikloridilla oli suuri tekninen merkitys, koska vinyylikloridi on monomeerinen rakennusosa PVC : n tuotannossa .
Nesteytys
Vesi lisää katalyyttien läsnä ollessa happamassa ympäristössä etyniä etenoliksi . Tämä tautomeerinen muoto järjestyy lopulta asetaldehydiksi ( keto-enolitautomerismi ).
Toisaalta terminaalialkyynit järjestyvät uudelleen hydraation jälkeen (myös tässä Markownikoff-säännön mukaan ), jolloin saadaan metyyliketoneja .
Luonnollinen esiintyminen
Alkyynit eivät ole luonteeltaan kovin yleisiä (tunnetaan vain 1000 yhdistettä), ja vain harvat niistä ovat fysiologisesti aktiivisia omassa organismissaan. Loput toimivat enimmäkseen sienitautien torjunta-aineina tai puolustusmyrkkyinä tai limakalvojen ärsyttäjinä. Esimerkiksi myrkyllisten tikka-sammakoiden iho erittää histrionikotoksiinia , ainetta, joka sisältää kaksi alkyyniryhmää ja suojaa sammakkoa nisäkkäiltä ja matelijoilta. Enediyne-antibiootit muodostavat suuren ryhmän biologisesti aktiivisia alkyynejä . Luonnolliset tuotteet , rakenteellinen motiivi enediyne laite on usein toimia sytotoksinen ihmisen kasvaimen solulinjojen ja siten edustaa potentiaalisia kemoterapeuttisia aineita. Eräs esimerkki on Streptomyces carcinostaticus eritettyjen neokarsinostatiini .
merkitys
Ainoastaan etyni (yleinen nimi asetyleeni) ja propyyni ovat teknisesti tärkeitä ; niitä käytetään muun muassa hitsauskaasuna, kun niiden liekit kuumenevat erittäin kuumaksi (jopa 3100 ° C). Etyylillä on suuri merkitys kemianteollisuudessa monien muiden yhdisteiden, kuten akryylihapon ja akryyliamidin, tuotannossa . Myös 2-butyni-1,4-dioli on esiaste tetrahydrofuraanin (THF) tuotannossa.
kirjallisuus
- Allinger , Cava , de Jongh , Johnson , Lebel , Stevens : Orgaaninen kemia , 1. painos, Walter de Gruyter, Berliini 1980, ISBN 3-11-004594-X , s.259-269.
- Beyer / Walter : Orgaanisen kemian oppikirja , 19. painos, S. Hirzel Verlag, Stuttgart 1981, ISBN 3-7776-0356-2 , s. 91-100.
- Morrison / Boyd : Orgaanisen kemian oppikirja , 3. painos, Verlag Chemie, Weinheim 1986, ISBN 3-527-26067-6 , s. 629-648.
- Streitwieser / Heathcock : Orgaaninen kemia , 1. painos, Verlag Chemie, Weinheim 1980, ISBN 3-527-25810-8 , s.363-383.
- K. Peter C.Vollhardt , Neil E.Schore : Orgaaninen kemia , 4. painos, Wiley-VCH, Weinheim 2005, ISBN 978-3-527-31380-8 , s. 631-661.
nettilinkit
Yksittäiset todisteet
- ↑ Merkintä alkyyneistä . Julkaisussa: IUPAC Compendium of Chemical Terminology ("kultakirja") . doi : 10.1351 / goldbook.A00236 Versio: 2.3 ..
- ↑ Hans-Dieter Jakubke, Ruth Karcher (toim.): Kemian sanasto, Spectrum Academic Publishing House, Heidelberg 2001.