Idiopaattinen interstitiaalinen keuhkokuume
| Luokitus ICD-10: n mukaan | |
|---|---|
| J84.1 | Muut interstitiaaliset keuhkosairaudet |
| ICD-10 verkossa (WHO-versio 2019) | |
Idiopaattinen interstitiaalinen pneumonia (IIP) muodostavat ryhmän harvinaisista aiheuttaman sairauden vaihtelevalla keuhkotulehduksen ( keuhkokuume ) ja arpeutuminen ( keuhkofibroosi ), pääasiassa sidekudosta keuhkojen ( interstitiumiin ) on osoitettu. Ne eroavat toisistaan taudin oireiden ( oireiden ), lähinnä kuvantamistestien , patologian , taudin kulun ja hoitovaihtoehtojen suhteen. Syy näiden kliinisten kuvien kehittymiselle ei ole tiedossa - siksi niitä kutsutaan " idiopaattisiksi ". IIP kuuluu suureen interstitiaalisen keuhkosairauden ryhmään (englanti: I nterstitial L ung D isease tai ILD), johon luokitellaan yli 200 erillistä sairautta . Interstitiaalisten keuhkosairauksien tärkein oire on hengenahdistus (hengenahdistus). Kaikki IIP-muodot johtavat vaihtelevan voimakkaaseen keuhkokuumeeseen, joka vaikuttaa ensisijaisesti keuhkojen sidekudokseen (interstitium) . Se voi myös aiheuttaa keuhkofibroosiksi kutsuttujen keuhkojen arpeutumista. Joissakin muodoissa keuhkofibroosi on etualalla ja tulehdus on vain mukana oleva reaktio. Ennustetta tai sairauden kulkua ja hoitovaihtoehdot riippuu muun muassa siitä, kuinka tärkeää on tulehdus tai fibroosia vastaavassa muodossa tauti.
luokittelu
Tässä esitetty (ei enää nykyinen) idiopaattisen interstitiaalisen keuhkokuumeen (IIP) luokitus perustuu American Thoracic Society (ATS) ja European Respiratory Society (ERS) yhdessä vuonna 2002 julkaisemaan ohjeeseen . Tämän luokituksen mukaan erotetaan seitsemän taudin muotoa, joista kukin määritellään erilaisilla kliinisillä, radiologisilla ja patologisilla kriteereillä. Lisäksi otettiin käyttöön luokka luokittelemattomille IIP: lle, johon on määritetty kaikki tapaukset, joita ei voida selkeästi rajoittaa:
- idiopaattinen keuhkofibroosi (IPF, idiopaattinen keuhkofibroosi) ,
- epäspesifinen interstitiaalinen keuhkokuume (NSIP) ,
- kryptogeeninen organisoiva keuhkokuume (COP) ,
- akuutti interstitiaalinen keuhkokuume (AIP) ,
- interstitiaalinen keuhkosairaus (RB-ILD) ,
- desquamative interstitial pneumonia (DIP) ja
- lymfoidinen interstitiaalinen keuhkokuume (LIP) .
Luokittelun merkitys on ennen kaikkea eri muotojen poikkitieteellisessä määrittelyssä, jonka patologit , radiologit ja internistit ovat tehneet pitkälti toisistaan riippumatta aikaisemmissa julkaisuissa . Tehtiin selväksi, että histopatologinen kuvio on erotettava kliinisestä diagnoosista. Luotettava kliininen diagnoosi perustuu kliinisiin, radiologisiin ja histopatologisiin havaintoihin. Vaikka luokituksen todistusaste on alhainen, koska se perustuu asiantuntijoiden havaintoihin, se muodostaa perustan tuleville tutkimuksille, koska tällä alalla on nyt yhtenäiset kriteerit.
Nykyinen luokitus on American Thoracic Society (ATS) ja European Respiratory Society (ERS) yhdessä julkaisema luokitus vuonna 2013.
Epidemiologia
Epidemiologiset tiedot idiopaattinen interstitiaalipneumonian eivät ole kovin luotettavia. Amerikkalainen työ kaikkien interstitiaalisten keuhkosairauksien (ILD) päällekkäisen ryhmän parissa tehtiin muun muassa New Mexicossa. Tämän tutkimuksen mukaan ILD: n esiintyvyys on 80 tapausta 100 000 asukasta kohden miehillä ja 67 tapausta 100 000 väestöä kohden naisilla. Keuhkofibroosin ja idiopaattisen keuhkofibroosin (IPF) diagnoosi on noin 45 prosenttia kaikista ILD-tapauksista.
Tämän tutkimuksen mukaan IPF: n esiintyvyys on 20 tapausta 100 000 asukasta kohden miehillä ja 13 tapausta 100 000 väestöä kohden naisilla. Koska tämä tutkimus tehtiin ennen uuden luokituksen julkaisemista, näiden tietojen oikeellisuus on kyseenalaista. Tuoreemmassa tutkimuksessa oletetaan olevan suurempi esiintyvyys. On todisteita siitä, että IPF kasvaa länsimaissa. Muiden IIP-muotojen epidemiologiaa on tutkittu vielä vähemmän.
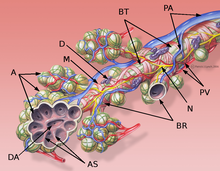
Anatomiset perusteet

PB : peribronkiaalinen sidekudos, BT : terminaalinen bronchiolus, M :keuhkoputkenpyöreä lihaskerros, P : keuhkovaltimon haara, DA : alveolaarinen kanava, A : alveolit, AS : alveolaarinen septa.
Värjäys hematoksyliini-eosiinilla (HE).
Interstitiumiin (interstitiaalinen kudos) on keuhko muodossa ns Interalveolarsepten välillä seinämien ilman pusseja (keuhkorakkuloiden). Viimeksi mainitut edustavat todellista toiminnallista keuhkokudosta ( parenkyymiä ), koska veren ja ilman välinen kaasunvaihto tapahtuu niissä . Interstitium on keuhkojen perusrakenne ja ylläpitää alveolien rakennetta ja siten veren ja ilman estettä hengitysjakson aikana. Interalveolaaristen väliseinien sidekudososa koostuu soluista, erityisesti sidekudoksen rakentajista ( fibroblasteista ), niiden muodostamista rakenneproteiineista ja aineista, kuten kollageenista , elastisista kuiduista , proteoglykaaneista ja muista glykoproteiineista .
Suurin osa interstitiumista koostuu kollageenikuiduista, jotka muodostavat jopa 20 prosenttia kuivasta keuhkomassasta. Keuhkojen interstitiumissa hallitsee tyypin I kollageeni, jonka uskotaan olevan tärkein rooli alveolien muodon ja joustavuuden ylläpitämisessä. Tyyppi IV esiintyy vain alveolien ja verisuonten kellarikerroksissa . Tyypin III ja V kollageenia muodostuu vain vähän (5-10 prosenttia) keuhkokudoksessa. Joustavat kuidut muodostavat haarautuneen verkon keuhkojen välissä. Ne ovat uloshengityksen ( vanhentumisen ) liikkeellepaneva voima .
Proteoglykaanit muodostavat interstitiumin perusaineen , ne varmistavat, että keuhkokudoksen tilarakenne säilyy. Niiden tarkkaa roolia keuhkojen toiminnassa ei tunneta yksityiskohtaisesti. Hyaluronihappoa , kondroitiinisulfaattia A ja C , dermataanisulfaattia , hepariinia ja hepariinisulfaattia löytyy keuhkoista . Muita glykoproteiineja ovat fibronektiini ja laminiini , joita esiintyy pääasiassa tyvikalvoissa.
Patogeneesi
Mekanismit, jotka edesauttaa sairauden kutsutaan kuin synnyssä . Idiopaattisessa interstitiaalisessa keuhkokuumeessa (IIP) keuhkokudoksen tulehduksella ja fibroosilla on ratkaiseva rooli. Heillä on erilainen asema eri muodoissa. Patogeneesiä ei kuitenkaan täysin ymmärretä.
tulehdus
Useimmissa interstitiaalisissa keuhkosairauksissa ja useimmissa idiopaattisissa interstitiaalisissa keuhkokuumeissa tulehdusreaktiolla näyttää olevan ratkaiseva rooli patogeneesissä. Mikroskooppinen tutkimus paljastaa tulehdussolujen ( makrofagit , granulosyytit ja lymfosyytit ) suuret kertymät näiden sairauksien keuhkokudoksessa , erityisesti alkuvaiheessa . Fibroosialueita esiintyy vain vähän ja loppuvaiheen keuhkofibroosia kehittyy vain harvoin. Keuhkofibroosi on sitten tulehdusreaktion seuraus. Tätä teoriaa vahvistaa se tosiasia, että sairaudet reagoivat hyvin anti-inflammatorisiin ja immunosuppressiivisiin hoitoihin. Keuhkofibroosia aiheuttavan tulehduksen poistaminen voi estää etenemisen.
Idiopaattinen keuhkofibroosi ja todennäköisesti myös akuutti interstitiaalinen keuhkokuume ovat erityisessä asemassa. Hypoteesi, jonka mukaan tulehduksellinen reaktio on ehto keuhkofibroosin kehittymiselle, ei näytä kestävän tässä. Tulehdusreaktiolla on tässä ilmeisesti toissijainen rooli tai se on vain mukana oleva reaktio keuhkofibroosiin.
Keuhkofibroosi
Keuhkofibroosi on reaktio, jossa se tulee arpeutuminen keuhkokudoksen. Eri solutyypeillä on tärkeä rooli keuhkofibroosin kehittymisessä. Sikäli kuin tiedämme tänään, tärkeimmät ovat fibroblasteja, endoteelisoluja ja alveolaarisia epiteelisoluja . Keuhkokudoksen vaurioitumisen jälkeen, jonka syytä idiopaattisessa interstitiaalisessa keuhkokuumeessa ei tunneta, fibroblastit joko ensin tulehtuvat ja sitten aktivoituvat tai aktivoituvat suoraan eli ilman edeltävää tulehdusta. Tämä riippuu käytettävästä mallista. Fibroblastien aktivaatio aloitetaan useilla lähettimillä, esimerkiksi kasvutekijöillä , kuten transformoiva kasvutekijä beeta 1 (TGF-p1) ja erilaisilla interleukiineilla , jotka vapautuvat muista soluista ja itse fibroblasteista. Tämä johtaa fibroblastien solujen lisääntymiseen ( lisääntymiseen ) sekä perusaineen ja sidekudoskuitujen uuteen muodostumiseen. Normaalisti tätä reaktiota säännellään tiukasti, mikä tarkoittaa, että vaurion tai haavan paranemisen jälkeen fibroblastien aktiivisuus estyy: toisaalta lähettimien alhaisemmalla vapautumisella ja toisaalta ohjelmoidulla solukuolemalla ( apoptoosi ) fibroblasteista. Nämä säätelymekanismit eivät toimi riittävästi keuhkofibroosissa. Tämä johtaa siihen, että muodostuu liikaa sidekudosta. Alveolaariset väliseinät laajenevat aiheuttaen kaasunvaihto- tai diffuusiohäiriön ( hengitysvajaus ). Lisäksi keuhkot menettävät joustavuutensa ( vaatimustenmukaisuuden ) ja voivat laajentua riittävästi vain sisäänhengityksen aikana lisääntyneen hengitystyön avulla. Kehitetään ns. Rajoittava ilmanvaihtohäiriö . Molemmat tekijät - kaasunvaihtohäiriö ja rajoittava ilmanvaihtohäiriö - johtavat keuhkofibroosin pääasialliseen oireeseen, hengenahdistukseen. Keuhkofibroosin edistyneissä vaiheissa fibroblastit siirtyvät myös alveolien onteloon, jossa ne myös muodostavat uuden sidekudoksen. Alveoleihin muodostuu fibroottisia alueita, jotka tunnetaan fibroottisina fokuksina . Tämä tuhoaa keuhkojen rakenteen näillä alueilla, johon liittyy täydellinen toiminnan menetys.
Oireet
Idiopaattisen interstitiaalisen keuhkokuumeen pääoire, kuten useimmat muut interstitiaaliset keuhkosairaudet, on hengenahdistus, joka esiintyy alkuvaiheessa vain fyysisen rasituksen yhteydessä. Koska IIP on tyypillisesti rajoittava ilmanvaihtohäiriö, kärsivillä on ensisijaisesti vaikeuksia hengittää sisään. Taudin edistyneellä vakavuudella ( etenemisellä ) hengenahdistus voi taudin muodosta riippuen esiintyä myös levossa ja loppuvaiheessa taudit voivat muuttua hengitysvajauksiksi. Keuhkofibroosille on ominaista myös kuiva yskä ilman expectoration .
Keuhkojen rajoitetusta toiminnasta kaasunvaihdon ja vaatimustenmukaisuuden vuoksi veressä voi esiintyä hapen puutetta, joka tunnetaan nimellä hypoksemia . Tämä voi ilmetä syanoosin muodossa , so . Violetista sinertävään ihon, limakalvojen ja kynsien värimuutokseen . Lisäksi kerhotoiminnan ja kellonlasi voivat muodostaa merkkinä hypoksemian. Vakavan hapenpuutteen sattuessa voi esiintyä myös tajunnan heikkenemistä .
diagnoosi
Perusdiagnostiikka
Lääketieteellinen historia ja fyysinen tutkimus
Tutkimuksen alussa on yksityiskohtainen sairaushistoria ( anamneesi ). Potilailta kysytään muun muassa heidän nykyisiä valituksiaan, tunnettuja sairauksia, ottamiaan lääkkeitä ja sukulaistensa sairauksia. Anamneesi on erittäin tärkeä, koska se auttaa sulkemaan pois muut sairaudet ja epäillyn diagnoosin. Monissa sairauksissa potilas kuvaa tyypillisiä oireita, joten epäilty diagnoosi osoittautuu usein oikeaksi lisätutkimusten jälkeen.
Frankfurter Bogen , joka on laajalle levinnyt saksankielisissä maissa, voi olla hyödyllinen keuhkosairauksien hoidossa . Potilas täyttää tämän lomakkeen ja ottaa huomioon melkein kaikki tärkeät näkökohdat, jotka ovat tärkeitä keuhkosairauksien yhteydessä. Idiopaattisen interstitiaalisen keuhkokuumeen oireet ovat epäspesifisiä. Kaikissa IIP-muodoissa esiintyvä hengenahdistus osoittaa, että voi olla keuhkosairaus, mutta se voi johtua myös lukuisista muista sairauksista, kuten sydänsairaudesta. Tämä pätee samalla tavalla kuin muut kuvatut oireet. IIP-diagnoosia tai epäiltyä diagnoosia ei sen vuoksi voida tehdä yksinomaan anamneesin perusteella.
Sairaushistoriaa seuraa yleensä yksityiskohtainen fyysinen tarkastus . Keuhkosairauksien kohdalla keskitytään koko kehon pinnan tarkasteluun ( tarkastamiseen ), rintakehän napauttamiseen ( lyömäsoittimet ) ja keuhkojen kuunteluun ( auskultointi ) stetoskoopilla . Ensisijaisesti fibroosille tyypilliset muutokset voidaan paljastaa IIP: n aikana fyysisellä tutkimuksella. Usein kuulokkeissa voi kuulla selkeän räiskyvän helisen , joka tunnetaan myös nimellä sklerofonia ja jolle on tunnusomaista hienokuplainen taustamelu, joka esiintyy sisäänhengityksen ja uloshengityksen loppupuolella. Perkussioiden avulla myös keuhkofibroosille tyypilliset korotetut keuhkorajat voidaan paljastaa. Syanoosin oireet, rumpukapulan sormet ja jo mainitut lasikynnet havaitaan tarkastuksen aikana. Fyysinen tutkimus ei salli luotettavaa diagnoosia myös IIP: ssä, mutta se voi edelleen rajoittaa mahdollisten sairauksien kenttää.
Tekniset tutkintamenettelyt
Epäiltyjen ILD- tai IIP-diagnostiikkojen perusdiagnostiikka sisältää tekniset tutkimukset, erityisesti keuhkotoiminnan ja rintakehän röntgenkuvan . Kehon pletysmografialla on tärkeä rooli keuhkojen toiminnan arvioinnissa . Keuhkofibroosi johtaa rajoittavaan ilmanvaihtohäiriöön, joka voidaan havaita tällä menetelmällä. Taudin alkuvaiheessa ei kuitenkaan välttämättä ole todisteita tällaisesta häiriöstä. Verikaasuanalyysiin ennen ja jälkeen fyysisen rasituksen sekä määrittämiseksi CO siirron tekijä voi saada viitteitä, kun läsnä on IIP jopa alkuvaiheessa. Molemmat tutkimusmenetelmät kuuluvat myös perusdiagnostiikan valikoimaan.
Fibroottiset muutokset voidaan tehdä näkyviksi myös keuhkojen röntgensäteillä. Myös tässä alkuvaiheen muutokset voivat olla niin pieniä, ettei niitä voida käyttää tavanomaisessa röntgendiagnostiikassa. Tyypillisiä merkkejä keuhkofibroosista röntgensäteillä ovat konsolidoituminen , vetovoima- bronkektaasia ja himmeä lasivarjoja. Konsolidoituminen johtuu alveolien fibroottisesta kudoksesta ja ne näkyvät röntgenkuvassa kirkkaina alueina, koska ne ovat elektronitiheitä kuin ilmatäytteiset alveolit. Traction bronchiectasis on keuhkoputkien laajeneminen ja johtuu niihin asetetusta jännitteestä, joka keuhkofibroosissa johtuu keuhkokudoksen kutistumisesta. Huurretut lasivarjot ovat myös kevyitä alueita, jotka johtuvat keuhkojen arkkitehtuurin tuhoutumisesta.
Lisädiagnostiikka
Jos perusdiagnoosin jälkeen epäillään IIP: tä kiireellisesti, suoritetaan yleensä erityinen tietokonetomografia (CT), joka tunnetaan nimellä korkean resoluution CT . Normaaliin CT: hen verrattuna tämä saavuttaa suuremman resoluution. HRCT: n avulla useimmat IIP-tapaukset voidaan tunnistaa suurella todennäköisyydellä ja taudin eri muodot voidaan erottaa. Keuhkofibroosin tyypilliset ominaisuudet CT: ssä maitolasilevytyksen ja Traktionsbronchiektasien ns. Hunajakenno keuhko tai lyhyt hunajakenno (engl. Honeycombing ) lisäksi. Kennosto keuhkojen kutsutaan koska sen samanlainen rakenne kuin hunajakenno . Hunajakennot syntyvät keuhkokudoksen rappeutumisen seurauksena.
Jos diagnoosi tai erottelu ei ole mahdollista tällä menetelmällä, on käytettävä invasiivisia tutkimusmenetelmiä. Ensimmäinen askel invasiivisia tutkimuksia on keuhkojen kanssa bronkoalveolaarinen huuhtelu (BAL) ja Transbronkiaalisia biopsia . Jos tämä ei myöskään sulje pois tai vahvista diagnoosia, on tehtävä torakotomia (avoin keuhkopiopsia ) tai videoavusteinen torakoskooppi ( VATS ), joka on kultainen standardi IIP: n diagnosoinnissa. Konsensuskonferenssin suositusten mukaan eri keuhkolohkoista tulisi ottaa vähintään kolme näytettä, joista jokaisen vähimmäiskoko on 2 cm.
hoito
Farmakologinen hoito
Idiopaattisen interstitiaalisen keuhkokuumeen (IIP) hoito suoritetaan olennaisesti kahdella lääkeryhmällä. Toisaalta glukokortikoidilla , kuten prednisolonilla , ja toisaalta niin kutsuttujen immunosuppressanttien , erityisesti atsatiopriinin ja syklofosfamidin kanssa . Lääkityksen tehokkuus riippuu potilaan kärsimän IIP-tyypistä. Vaikka idiopaattisen keuhkofibroosin (IPF) ja akuutin interstitiaalisen keuhkokuumeen (AIP) farmakologisella hoidolla ei ole tai on vain väliaikainen vaikutus taudin kulkuun, muut muodot reagoivat hyvin tulehduskipulääkkeisiin, jolloin paraneminen tapahtuu tai ainakin keskimääräistä eloonjäämisaikaa voidaan pidentää huomattavasti.
Tulehduskipulääkkeiden erilaiset vastaukset johtuvat todennäköisesti eri muotojen erilaisesta patogeneesistä . Nykytutkimuksen mukaan fibroosi on etusijalla IPF: ssä ja AIP: ssä ja tulehdusreaktio on vain mukana oleva reaktio tai sen seuraus. Toisaalta muussa muodossa keuhkovälitulehdus määrää taudin kulun ja jonka fibroosi on vain taudin loppuvaiheessa.
IPF: n ja AIP: n hoitoon kohdistetaan suuria toiveita aineisiin, jotka voivat estää fibroosin etenemisen, ts. Fibroblastien solujen lisääntymisen ja kollageenisynteesin. Suuri määrä tällaisia aineita on tällä hetkellä (2008) kliinisissä tutkimuksissa . Niitä ei kuitenkaan ole vielä hyväksytty tavalliseen IIP-hoitoon.
Keuhkosiirto
Keuhkosiirrännäisen voidaan harkita, jos vahingontutkimusajanjaksolla tai keuhkofibroosi on loppusuoralla ja ei reagoi lääkehoitoa. Keuhkosiirto lisää eloonjäämisastetta edenneessä keuhkofibroosissa. Yhden keuhkon siirtäminen vastaa kahden keuhkon siirtämistä. Indikaatiota keuhkosiirrolle ei usein tehdä ajoissa. Tutkimuksen mukaan, johon osallistui 1376 potilasta, yli 30 prosenttia kuoli odottamisesta kauan ennen kuin keuhkosiirto voidaan suorittaa.
Kliiniset erot idiopaattisessa interstitiaalisessa keuhkokuumeessa
Idiopaattinen keuhkofibroosi (IPF)
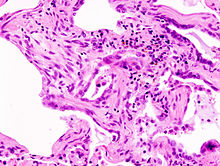
Idiopaattinen keuhkofibroosi tai idiopaattinen keuhkofibroosi on yleisin ajanjaksona ja on pahin ennuste. Keskimääräinen eloonjäämisaika diagnoosin jälkeen on keskimäärin kolme vuotta ja viiden vuoden eloonjäämisaste on 20-40 prosenttia. Potilaat ovat yleensä yli 60-vuotiaita diagnoosin tekohetkellä ja miehet kärsivät hieman useammin kuin naiset. Esiintyvyys on noin 6/100000.
Morfologiset muutokset ovat pääasiassa paikallisia keuhkopohjan alueella, ts. Keuhkojen alaosassa. Tyypillinen histologinen kuvio IPF kutsutaan U sual I nterstitial P neumonia nimetty (UIP, tavallinen interstitiaalinen keuhkokuume), ja on tunnettu siitä, että hajanaista fibroosia sekä kennomainen rakenne keuhkoihin. UIP: n malli on tyypillinen, mutta ei spesifinen, IPF: lle ja löytyy myös muista interstitiaalisista keuhkosairauksista. Taudin edistyneissä vaiheissa röntgenkuva näyttää tyvisolukerroksen (retikulaarisen) verisuonirakenteen. In HRCT (korkea resoluutio tietokonetomografia) luistonesto keuhkoputkien laajentuma ja kennot, joissa on perus- ja subpleural jakelu ovat tyypillisiä.
IPF-taudin puhkeaminen on salakavalaa, ja sille on ominaista lisääntyvä hengenahdistus, kuiva, ärtyisä yskä ja rätinä keuhkojen auskultaatiossa. IPF voi myös sattua nykyisten keuhkosairaudet, esimerkiksi yhdistettynä keuhkolaajentuma vuonna COPD ; Tupakointi on myös riskitekijä IPF: lle. IPF ei yleensä reagoi glukokortikoidihoitoon edes yhdessä immunosuppressiivisten lääkkeiden kanssa. Keuhkojensiirtoa pidetään tehokkaana terapeuttisena toimenpiteenä erikoistapauksissa. Pirfenidoni (kauppanimi Esbriet® ) on hyväksytty lääkkeeksi EU: ssa vuodesta 2011 ja Yhdysvalloissa vuodesta 2014 tapauksiin, jotka eivät ole vielä kovin pitkälle edenneet. Alkuperäisten tietojen mukaan tämä vaikuttava aine hidastaa taudin kulkua; Yleisiä haittavaikutuksia ovat huimaus, pahoinvointi, ihottuma, lisääntynyt ihon herkkyys valolle. Vuonna 2015 nintedanibi (kauppanimi Ofev® ) hyväksyttiin kaikille IPF: n taudin vaiheille Yhdysvalloissa ja Euroopassa.
Epäspesifinen interstitiaalinen keuhkokuume (NSIP)
Ei-spesifinen interstitiaalinen pneumonia (NSIP) on alle idiopaattinen interstitiaalinen keuhkokuume (IIP), toiseksi yleisin ja varianttien muodossa. Potilaat ovat enimmäkseen 50-60-vuotiaita ja siten keskimäärin hieman nuorempia kuin IPF-potilaat. Naiset ja miehet kärsivät tasapuolisesti.
NSIP: llä ei ole tyypillistä lokalisointia morfologisten muutosten suhteen. Pikemminkin muutokset ovat homogeenisia ja jakautuvat enimmäkseen symmetrisesti koko keuhkoihin. Histologista mallia kutsutaan myös NSIP: ksi. NSIP: ssä on kaksi alaryhmää (alatyyppiä), solu ja fibroottinen alatyyppi. Solutyypissä histologista ulkonäköä hallitsevat tulehdussolut; fibroottisessa alatyypissä esiintyy myös voimakkaita fibroosialueita. Histologisen kuvan tavoin radiologisessa kuvassa on myös runsaasti vaihteluita. Hajautuneesti jakautuneiden maitolasin opasiteettien lisäksi on mikromoduuleja ja hunajakennoja. Edistyneissä vaiheissa normaalia keuhkorakennetta on vaikea nähdä röntgen- ja TT-kuvissa, koska se on tuhoutunut bronkektaasien, kystien ja konsolidoitumisten avulla.
NSIP: n oireet eroavat vain vähän IPF: n oireista. Se näyttää kuitenkin lievemmältä, etenee hitaammin ja sillä on parempi ennuste. Ennuste riippuu myös histologisesta alatyypistä ja on parempi solutyypille kuin fibroottiselle alatyypille, koska tämä reagoi paremmin tulehduskipulääkkeisiin. Kaiken kaikkiaan lääkehoito on paljon lupaavampaa kuin IPF: n tapauksessa. Koska NSIP: n morfologiset muutokset ovat niin vaihtelevia, diagnoosi on lääkäreille vaikein verrattuna muihin IIP: iin. Tämä pätee erityisesti fibroottiseen alatyyppiin.
Kryptogeeninen organisoiva pneumonia (COP)
Koska kryptogeeninen organisoiva keuhkokuume ( kryptogeeninen organisoiva keuhkokuume ) viitataan kliiniseen kuvaan, kliiniset, radiologiset ja patologiset piirteet ovat melko ominaisia. Kuten NSIP: n kohdalla, COP: ssä ei ole sukupuolivalintaa ja potilaiden keski-ikä on 50-60 vuotta. Tupakoimattomat kärsivät noin kaksi kertaa useammin kuin tupakoitsijat. Tämän tilastollisen poikkeavuuden syytä ei tunneta.
Histologista mallia kutsutaan organisoivaksi keuhkokuumeeksi (OP). Sille on ominaista rakeistuskudoksen ulkonäkö, joka täyttää keuhkoputket ja alveolit. Nämä muutokset eivät tuhoa keuhkojen parenkyymiä. Tätä mallia esiintyy harvoin idiopaattisessa muodossa. Usein muut sairaudet voidaan pitää vastuussa näistä muutoksista toissijaisena syynä, esimerkiksi kollagenoosit ja tartuntataudit tai lääkkeiden aiheuttamat sairaudet. Samanlainen histologia esiintyy bronkioliitissa obliterans . Tästä syystä COP tunnettiin aiemmin nimellä keuhkokuumetta organisoiva bronkioliitti obliterans (BOOP) . Tätä termiä ei enää käytetä, jotta vältetään sekaannus bronkioliitti obliterans -lajin riippumattoman kliinisen kuvan kanssa. Rakeistuskudos näkyy röntgen- ja TT-kuvissa ns. Konsolidointialueiden muodossa , jotka sijaitsevat pääasiassa keuhkoputkien ympärillä (peribronchial) ja suoraan pleuran alla (subpleural). Pinnoitusten ympärillä voi esiintyä himmeää lasia.
Kliininen kuva alkaa yleensä yleisillä oireilla, kuten huonovointisuus, kuume , laihtuminen ja kuiva yskä. Oireet lisääntyvät yhden tai kolmen kuukauden kuluessa. COP voidaan hoitaa hyvin glukokortikoidilla ja sillä on hyvä ennuste. Usein tauti puhkeaa uudelleen hoidon lopettamisen jälkeen. Tätä kutsutaan uusiutumiseksi . Jos uusiutuu, tauti voidaan hoitaa uudelleen glukokortikoidilla.
Akuutti interstitiaalinen keuhkokuume (AIP)
In Toisin kuin muut idiopaattinen interstitiaalinen pneumonia (IIP), akuutti interstitiaalinen pneumonia (AIP) on akuutti kurssi. Sille on ominaista äkillinen oireiden ilmaantuminen ja se johtaa usein asteittaiseen hengityshäiriöön ( hengitysvajaus ). Taudilla on huonoin ennuste IIP: stä. Kurssi on kohtalokas yli puolessa tapauksista. Suurin osa kuolemista tapahtuu yhden tai kahden kuukauden kuluttua taudin alkamisesta.
AIP: n puhkeamista edeltää usein ylempien hengitysteiden infektio , jolle voi olla tunnusomaista yleinen sairauden tunne, raajojen kipu , kuume ja vilunväristykset. Sitten potilaalle kehittyy hengenahdistus (hengenahdistus) muutamassa päivässä, mikä ilmenee aluksi vain liikunnan aikana. Hapen puute veressä (hypoksemia) voidaan havaita jo alkuvaiheessa. Toinen ominaisuus on selkeä rätinä, joka on arvioitava merkiksi konsolidoitumisesta rajoittavan ilmanvaihtohäiriön yhteydessä. Hapen puute veressä ( hypoksemia ) kehittyy muutamassa viikossa levottomaksi hengenahdistukseksi (levottomaksi hengenahdistukseksi), joka voi muuttua hengitysvajaukseksi. Tässä vaiheessa potilaalle on annettava happea ja tietyissä olosuhteissa koneellisesti tuuletettava.
Histologinen kuvio on sama kuin diffuusi alveolaarivaurio (engl. Diffuse alveolaaravaurio , lyhyt - DAD ), jota ei voida erottaa akuutin aikuisen hengitysvaikeusoireyhtymän patologisista muutoksista (engl. Akuutti hengitysvaikeusoireyhtymä , lyhyt ARDS ). AIP ja ARDS eroavat vain syystä. Vaikka ARDS esiintyy pääasiassa sepsiksen tai sokin yhteydessä , AIP: n syytä ei tunneta. Louis Virgil Hamman ja Arnold Rice Rich kuvasivat vastaavia tapauksia jo 1940-luvulla, jotka myöhemmin tiivistettiin Hamman-Richin oireyhtymäksi . Todennäköisesti nämä tapaukset kuvaavat nykyistä AIP: tä.
Hengityselinten keuhkoputkentulehdus, interstitiaalinen keuhkosairaus (RB-ILD) ja desquamative interstitial pneumonia (DIP)
Kun hengityselinten keuhkoputkentulehdus interstitiaalinen keuhkosairaus ja desquamative interstitiaalinen keuhkokuume on sairaus, jolla on samanlainen mutta erottuva ulkonäkö. Molempia sairauksia esiintyy pääasiassa, yksinomaan RB-ILD: tä ja DIP: tä yleensä tupakoitsijoilla. Keskimääräinen puhkeamisen ikä on noin 40–50 vuotta, ja miehet kärsivät siitä kaksi kertaa useammin kuin naiset. RB-ILD on oireenmukaiseen variantti hengitysteiden bronkioliitti, tulehdus, keuhkoputkia , että löytyy säännöllisesti sattumalta tupakoitsijoilla. Oireettoman ja oireenmukaisen variantin histologista mallia kutsutaan myös hengityselinten bronkioliitiksi (RB).
Jotkut asiantuntijat pitävät DIP: tä RB-ILD: n edistyneenä muunnoksena. Tämä on kuitenkin epäilyttävää, koska DIP, toisin kuin RB-ILD, esiintyy toisinaan myös tupakoimattomilla ja huomattavien morfologisten erojen vuoksi (ks. Alla). Tästä epävarmuudesta johtuen konsensusluokitus mahdollistaa näiden kahden vaihtoehdon erottamisen. Termi DIP otettiin käyttöön vuonna 1969 Liebow ja Carrington väärällä olettamuksella, että nämä soluryhmät olivat kuorintoja alveolaarisesta epiteelistä. Tämä kuorinta solujen kutsutaan hilseily (latinan squama "asteikot"). Termi DIP on kuitenkin säilynyt nykyisessä luokituksessa osittain siksi, että DIP on harvinaisuus eikä sitä ole korvattu sopivammalla termillä alveolaarinen makrofagipneumonia . DIP: n histologista mallia kutsutaan myös DIP: ksi.
Molempien muotojen histologiselle kuvalle on ominaista lukuisat ruskeapigmentoitujen makrofagien kertymät keuhkoihin. RB-ILD, pigmentoitu makrofageja sijaitsevat pääasiassa luumenissa bronchioles (bronchiolocentrically), kun taas DIP ne tavataan etupäässä luumeneita keuhkorakkuloihin (intraalveolar). Lievä fibroosi on myös tyypillistä DIP: lle. Nämä kaksi kliinistä kuvaa eroavat myös morfologisten muutosten jakautumisesta. Vaikka RB-ILD: tä esiintyy pääasiassa keuhkojen ylemmissä lohkoissa, DIP: llä on edullinen subpleraalinen lokalisointi ja hallitsevuus alemmissa lohkoissa. Tämä jakautumismalli on erityisen helppo havaita HRCT: ssä. Niin sanotut keskilobulaariset kyhmyt ovat ominaisia RB-ILD: lle ja himmeät lasivarjot DIP: lle.
Kliinisille oireille on tunnusomaista hengenahdistuksen ja kuivan, kutittavan yskän hidas kehittyminen. Rumpukapulan sormet löytyvät myös noin puolelta potilaista. Molemmat muodot reagoivat hyvin glukokortikoideihin ja niillä on hyvä ennuste. Vain harvoissa tapauksissa DIP kehittää hengitysvajausta, jolla on korkea kuolleisuus.
Lymfoidinen interstitiaalinen pneumonia (LIP)
LIP esiintyy ensisijaisesti naisilla, joiden ikähuippu on noin 50 vuotta. Idiopaattisessa muodossa LIP on harvinaisin IIP. Sitä esiintyy paljon useammin toissijaisena esiintymänä autoimmuunisairauksien ja immuunipuutoksen yhteydessä .
Histologista mallia, kuten kliinistä diagnoosia, kutsutaan LIP: ksi, ja sille on tunnusomaista alveolaaristen väliseinien tunkeutuminen lymfosyytteihin ja makrofageihin sekä imusolmukkeiden peribronkiaalinen muodostuminen . Muutokset ovat hajautuneita koko keuhkoissa. HRCT: ssä himmeät lasivarjot ovat tyypillisiä.
Potilailla on vain lieviä oireita, ja he kärsivät pääasiassa lievästä hengenahdistuksesta ja yskästä. Toissijaisissa muodoissa taustalla olevan taudin oireet ovat etualalla. Harvoissa tapauksissa LIP voi kehittyä keuhkofibroosiksi tai pahanlaatuiseksi lymfoomaksi . Tämän komplikaation lisäksi LIP: llä on hyvä ennuste. Hoito suoritetaan yleensä glukokortikoideilla, joiden tehokkuutta tässä IIP-muodossa ei ole vielä osoitettu satunnaistetuilla tutkimuksilla.
Idiopaattinen interstitiaalinen keuhkokuume eläimillä
Eläinten idiopaattisen interstitiaalisen keuhkokuumeen ryhmää ei ole toistaiseksi tutkittu vähän. Siksi perustutkimuksiin ei ole sopivaa mallieläintä - jyrsijöiden bleomysiinin aiheuttama keuhkofibroosi on vain sairaus, joka on ( fenomenologisesti ) samanlainen ulkonäöltään , mutta ei täytä riittävän mallin vaatimuksia.
Tällaisia kroonisia idiopaattisia sairauksia voi esiintyä useammin joillakin terrierirotuilla ( West Highland White Terriers , Staffordshire Bull Terriers , Scottish Terriers ). Koiran idiopaattinen keuhkofibroosi esiintyy pääasiassa vanhemmat eläimet ja vastaa kryptogeeninen järjestävän keuhkokuume ihmisillä. Kirjallisuudessa kissoilla on kuvattu vain muutamia IIP-tapauksia; tuoreen tutkimuksen mukaan se vastaa ihmisen idiopaattista keuhkofibroosia (IPF) ja johtuu todennäköisesti tyypin II pneumosyyttien puutteesta .
Tähän mennessä lintujen sinirintaisesta papukaijasta on vain yksi raportti .
Tutkimushistoria
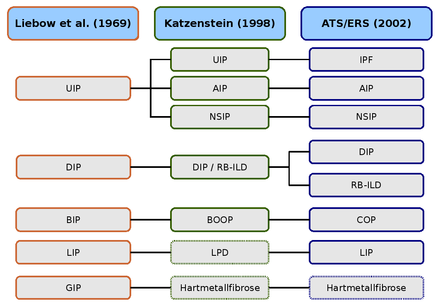
AIP (akuutti interstitiaalinen keuhkokuume),
BIP (bronkoliittinen interstitiaalinen keuhkokuume),
BOOP (bronkioliitti obliterans, jossa on järjestyvä keuhkokuume),
COP (kryptogeeninen interstitiaalinen keuhkokuume),
DIP (desquamatiivinen interstitiaalinen keuhkokuume),
GIP (jättisolupneumonia),
LPD (lymfoproliferatiiviset sairaudet),
LIP (lymfoidinen interstitiaalinen keuhkokuume),
NSIP ( epäspesifinen interstitiaalinen keuhkokuume),
RB-ILD (hengityselinten bronkioliitti ja interstitiaalinen keuhkosairaus),
UIP (tavallinen interstitiaalinen keuhkokuume).
Ensimmäinen kuvaus interstitiaalisesta keuhkosairaudesta juontaa juurensa vuoteen 1892 ja on peräisin kanadalaisesta lääkäriltä William Oslerilta . Hän tunnusti jo monipuolisen ulkonäön ja huomautti muutosten edelleen luokittelun tarpeellisuuden ja vaikeuden.
Sisätautien Louis Vergilius höyrysauna ja patologi Arnold Rice Rich raportoitiin vuonna 1944 neljä potilaan tapauksissa vaikuttaa akuutti diffuusi interstitiaalinen fibroosi. Hamman-Rich oireyhtymä on nimetty heidän. Tätä termiä käytettiin sitten jonkin aikaa kaikkiin sairauksiin, joissa esiintyi kroonista diffuusi keuhkofibroosia tuntemattomalla syyllä, vaikka kuvatut tapaukset olivatkin akuutteja. Kirjoittajat kuvailivat todennäköisesti sitä, mitä nyt kutsutaan akuutiksi interstitiaaliseksi keuhkokuumeeksi.
Ensimmäinen idiopaattisten interstitiaalisten keuhkosairauksien histologinen luokitus tulee kahdelta patologilta Averill Abraham Liebow ja Charles B.Carrington (1969). Tuolloin luokittelussa erotettiin viisi histologista mallia, jotka sisällytettiin ensin sateenvarjo-termiin idiopaattinen keuhkofibroosi . Höyrysaunassa-Rich oireyhtymä oli akuutti variantti " U sual I nterstitial P luokitellut neumonia" (UIP, tavallinen interstitiaalinen pneumonia).
Liebow-Carrington-luokitusta kehitettiin edelleen vuonna 1997 Anna-Luise A. Katzensteinin toimesta ja vuonna 1998 yhteistyössä Jeffrey L. Myersin kanssa ja sovitettiin tutkimuksen nykytilaan. Syy " G Iant I nterstial P neumonia" (GCP, jättisoluartriitti keuhkokuume) on nyt selvitetty. Se laukaisee metallipölyn hengittämisen ja tunnetaan kovametallifibroosina . Lymfoidinen interstitiaalinen keuhkokuume määritettiin "lymfoproliferatiivisille sairauksille" (LPD, lymfoproliferatiiviset sairaudet).
Yksittäiset todisteet
- Huomautus : Ellei toisin mainita, artikkeli perustuu vuoden 2002 konsensuskonferenssin julkaisuun: American Thoracic Society / European Respiratory Society International Multidisciplinary Consensus Classification of Idiopathic Interstitial Pneumonias. Julkaisussa: Am J Respir Crit Care Med. 165 (2), 15. tammikuuta 2002, s.277--304. PMID 11790668 . doi : 10.1164 / ajrccm.165.2.ats01 .
- ↑ a b c d American Thoracic Society / European Respiratory Society International Multidisciplinary Consensus Classification of Idiopathic Interstitial Pneumonias. Julkaisussa: Am J Respir Crit Care Med. 165 (2), 15. tammikuuta 2002, s.277--304. PMID 11790668 . doi : 10.1164 / ajrccm.165.2.ats01 .
- ↑ GW Hunninghake, MI Black: Huipputason tekniikka. Selittääkö nykyinen tieto idiopaattisen keuhkofibroosin patogeneesiä? Julkaisussa: Proc Am Thorac Soc. 4 (5), syyskuu 2007, s.449-452. PMID 17684287 . doi : 10.1513 / paid.200702-036MS .
- ^ KO Leslie: Historiallinen näkökulma: patologinen lähestymistapa idiopaattisten interstitiaalisten keuhkokuumeiden luokitteluun. Julkaisussa: Chest. 128 (5 Suppl 1), marraskuu 2005, s. 513S-519S. PMID 16304241 . doi : 10.1378 / chest.128.5_suppl_1.513S .
- ↑ U. Costabel: Idiopaattinen interstitiaalikeuhkokuume - miksi toinen konsensus luokitus? Julkaisussa: Pneumology. 56, 2002, s.279-280. doi : 10.1055 / s-2002-30703 .
- ↑ Gerd Herold ja kollegat: Sisätautilääkärit 2021. Oma julkaisu, Köln 2021, ISBN 978-3-9821166-0-0 , s.393 .
- ^ DB Coultas et ai.: Interstitiaalisten keuhkosairauksien epidemiologia. Julkaisussa: Am. J. Respir. Crit. Care Med. Vol 150, nro 4, 10, 1994, s. 967 - 972. doi : 10.1164 / ajrccm.150.4.7921471 .
- ↑ G. Raghu et ai .: Idiopaattisen keuhkofibroosin ilmaantuvuus ja esiintyvyys. Julkaisussa: Am J Respir Crit Care Med. 174 (7), 1. lokakuuta 2006, s.810-816. Epub 2006, kesäkuu 29. PMID 16809633 . doi : 10.1164 / rccm.200602-163OC .
- ^ Francis HY Green: Katsaus keuhkofibroosiin. Julkaisussa: Chest. 122, 2002, s. 334S-339S. doi : 10.1378 / chest.122.6_suppl.334S .
- ^ JE Gadek et ai: Sidekudoksen proteaasien rooli kroonisen tulehduksellisen keuhkosairauden patogeneesissä. Julkaisussa: Environ Health Perspect . 55, huhtikuu 1984, s. 297-306. PMID 6329673 . doi : 10.1289 / ehp.8455297 .
- ^ TE King: Idiopaattiset interstitiaaliset keuhkokuumeet: edistyminen luokittelussa, diagnoosissa, patogeneesissä ja hoidossa. Julkaisussa: Trans Am Clin Climatol Assoc. 115, 2004, s. 43-78. PMID 17060957 .
- ↑ Gross et ai.: Idiopaattinen keuhkofibroosi. Julkaisussa: N Engl J Med . 345, 2001, sivut 517-525. doi : 10.1056 / NEJMra003200 .
- ^ BC Willis et ai .: Myofibroblastien epiteelinen alkuperä keuhkofibroosin aikana. Julkaisussa: Proc Am Thorac Soc. 3 (4), kesäkuu 2006, s. 377-382. PMID 16738204 . doi : 10.1513 / pats.200601-004TK .
- ↑ R. Klinke, S. Silbernagl (Toim.): Fysiologian oppikirja. 4. painos. Thieme-Verlag, 2003, ISBN 3-13-796004-5 .
- ↑ M. Dietel et ai.: Harrisonin sisätautien. 15. painos. ABW Wissenschaftsverlag, Berliini 2003, ISBN 3-936072-10-8 .
- ↑ H.Kronenberger et ai .: Uusi kyselylomake keuhko- ja hengitystiesairauksien kirjaamiseksi. Julkaisussa: Prax. Clin. Pneumol. 39, 1985, sivut 241-251.
- B a b c Günther et ai .: Idiopaattisen interstitiaalisen keuhkokuumeen luokittelu, diagnoosi ja hoito: kriittinen luettelo Saksassa tällä hetkellä harjoitetusta käytännöstä. Julkaisussa: Deutsches Ärzteblatt. 24. kesäkuuta 13. kesäkuuta 2003 ( html-versio ), (PDF-versio) ( Memento 30. heinäkuuta 2004 alkaen Internet-arkistossa ).
- B a b Kauffmann et ai .: Radiologia. 3. painos. Urban & Fischer Munich / Jena 2006, ISBN 3-437-44415-8 .
- ↑ U. Costabel et ai .: keuhkofibroosit - luokittelu, diagnoosi, hoito. Julkaisussa: Internist. [Suppl 1] 44, 2003, s. S35-S43. doi : 10.1007 / s00108-003-0977-6 .
- ↑ JD Hosenpud et ai .: Diagnoosin vaikutus keuhkosiirron eloonjäämisen hyötyyn loppuvaiheen keuhkosairaudessa. Julkaisussa: The Lancet . 351 (9095), 3. tammikuuta 1998, s. 24-27. PMID 9433425 . doi : 10.1016 / S0140-6736 (97) 06405-2 .
- ↑ BF Meyers et ai .: Yhden tai kahdenvälinen keuhkosiirto idiopaattisen keuhkofibroosin hoitoon: kymmenvuotinen institutionaalinen kokemus. Julkaisussa: J Thorac Cardiovasc Surg . 120, 2000, s. 99-107. PMID 10884661 . doi : 10.1067 / mtc.2000.106322 .
- ^ J. De Meester et ai .: Keuhkojensiirron odotuslista: loppuvaiheen keuhkosairauden tyypin ero vuoden kuluttua rekisteröinnistä. Julkaisussa: J Heart Lung Transplant . 18 (6), kesäkuu 1999, s. 563-571. PMID 10395354 . doi : 10.1016 / s1053-2498 (99) 00002-9 .
- ^ DS Kim et ai: Idiopaattisten interstitiaalisten keuhkokuumeiden luokittelu ja luonnehistoria. Julkaisussa: Proc Am Thorac Soc. 3 (4), kesäkuu 2006, s.285-292. PMID 16738191 . doi : 10.1513 / pats.200601-005TK .
- ↑ David A Lynch, Nicola Sverzellati, William D Travis, Kevin K Brown, Thomas V Colby: Diagnostiset kriteerit idiopaattiselle keuhkofibroosille: Fleischner Society White Paper . Julkaisussa: The Lancet Respiratory Medicine . nauha 6 , ei. 2. helmikuuta 2018, s. 138-153 , doi : 10.1016 / S2213-2600 (17) 30433-2 .
- ↑ PW Noble et ai .: Pirfenidoni potilailla, joilla on idiopaattinen keuhkofibroosi (KAPASITEETTI): kaksi satunnaistettua tutkimusta. Julkaisussa: Lancet. 377 (9779), 21. toukokuuta 2011, s. 1760-1769. doi: 10.1016 / S0140-6736 (11) 60405-4 . Epub 2011 13. toukokuuta.
- ^ H. Monaghan et ai.: Histologisten mallien ennustevaikutukset useissa kirurgisissa keuhkopoikeissa potilaista, joilla on idiopaattinen interstitiaalinen keuhkokuume. Julkaisussa: Chest. 125 (2), helmikuu 2004, s. 522-526. PMID 14769733 . doi : 10.1378 / rinnassa.125.2.522 .
- ↑ Katso myös Joachim Frey : Hengityselinten sairaudet. Julkaisussa: Ludwig Heilmeyer (Hrsg.): Sisätautien oppikirja. Springer-Verlag, Berliini / Göttingen / Heidelberg 1955; 2. painos ibid. 1961, s. 599-746, tässä: s. 708 ( Diffuusi progressiivinen interstitiaalinen keuhkofibroosi : keuhkofibroosi (Hamman-Rich 1944)).
- B a b K.Williams et ai.: Spontaanin kissan idiopaattisen keuhkofibroosin tunnistaminen: morfologia ja ultrastruktuuriset todisteet tyypin II pneumosyyttivirheestä. Julkaisussa: Chest. 125 (6), kesäkuu 2004, s. 2278-2288. PMID 15189952 . doi : 10.1378 / rinnassa.125.6.2278 .
- ^ BM Corcoran et ai .: Krooninen keuhkosairaus Länsi-Ylämaan valkoisilla terriereillä. Julkaisussa: Vet Rec. 144 (22), 29. toukokuuta 1999, s. 611-616. PMID 16119057
- ↑ LA Cohn et ai .: Idiopaattisen keuhkofibroosin kaltaisen tilan tunnistaminen ja karakterisointi kissoilla. Julkaisussa: J Vet Intern Med. 18 (5), syys-lokakuu 2004, s.632-641. PMID 15515577 . doi : 10.1111 / j.1939-1676.2004.tb02598.x .
- ↑ O. Amann et ai.: Krooninen keuhkosairaus interstitiaalinen fibroosi sininen verhottujen Amazon papukaijan (Amazona Aestiva Aestiva). Julkaisussa: Avian Dis. 51 (1), maaliskuu 2007, s.150-153. PMID 17461284 . doi : 10.1637 / 0005-2086 (2007) 051 [0150: CPIFIA] 2.0.CO; 2 .
- ↑ A. Katzenstein, J. Myers: idiopaattinen keuhkofibroosi - kliininen merkitys Patologinen luokittelu. Julkaisussa: Am J Respir Crit Care Med. 157 (4 Pt 1), huhtikuu 1998, s. 1301-1315. PMID 9563754 . doi : 10.1164 / ajrccm.157.4.9707039 .
- ^ R. Collard et ai .: Demystifioiva idiopaattinen interstitiaalinen pneumonia. Julkaisussa: Arch Intern Med . 163, 2003, s. 17--29. PMID 12523913 . doi : 10.1001 / archinte.163.1.17 .
kirjallisuus
- J. Müller-Quernheim: Interstitiaaliset keuhkosairaudet . Thieme, Stuttgart 2001, ISBN 3-13-132281-0 .
- H. Schweisfurth et ai: Kuinka interstitiaaliset keuhkosairaudet diagnosoidaan Saksassa? Julkaisussa: Pneumology. 57, 2003, s. 373-382. doi: 10.1055 / s-2003-40557