Klorofyylit
Klorofylli (alkaen vanha kreikkalainen χλωρός Chloros "vaaleanvihreä, tuore" ja φύλλον phyllon "lehtiä") tai lehvistönvihreä viittaa luokan luonnon väriaineita , jotka on muodostettu organismeja, jotka fotosynteesi toimivat. Erityisesti kasvit saavat vihreän värinsä klorofyllistä.
Kasveilla, levillä ja syanobakteereilla on erityyppisiä klorofylliä, fotosynteesiä johtavilla bakteereilla on erityyppisiä bakterioklorofylliä .
Rakenne ja ominaisuudet
Klorofyylit ovat molekyylirakenteita, joita kutsutaan kelaattikomplekseiksi ja jotka koostuvat derivatisoidusta porfyriinirenkaasta ja Mg 2+ : sta keski-ionina. Toisin kuin porfyriinissä, klorofylylien perusrakenne sisältää toisen, viidennen renkaan renkaassa III (numerointi Fischerin mukaan). Klorofyllityypistä riippuen eri sivuketjut kiinnitetään runkoon. Esimerkiksi, klorofylli a: esteröity kanssa phytol (katso taulukko). Klorofyllidit ovat klorofylleja ilman sivuketjuja.
Rakenteellisesti klorofyylit liittyvät hemiin , jota esiintyy veripigmentin ( hemoglobiini ), myoglobiinin ja sytokromien komponenttina , mutta keski-ionina eivät sisällä magnesiumia, vaan rautaa . Klorofyylit liukenevat helposti etanoliin ja asetoniin samoin kuin vastaaviin liuottimiin. Jos fotosynteesi tapahtuu organismeissa, jotka vapauttavat happea (happiset fototrofit ), puhutaan yleensä klorofyllistä . Hapettomat fototrofit eivät kuitenkaan tuota happea reaktiotuotteena fotosynteesin aikana, näissä organismeissa klorofylliä kutsutaan bakterioklorofylliksi .
Hans Fischer määritti klorofyllin molekyylirakenteen vuonna 1940, absoluuttisen kokoonpanon selvitti Ian Fleming vuonna 1967 .
Happipitoisten fototrofien kemiallinen rakenne
| Sukunimi | rakenne | C 2 loppuosa | C 3 loppuosa | C 7 loppuosa | C 8 loput | C 17 loput | C 17-18- sidos | Molekyylikaava |
|---|---|---|---|---|---|---|---|---|
| Klorofylli a |

|
-CH 3 | -CH = CH 2 | -CH 3 | CH 2 CH 3 | CH 2 CH 2 COO- fytyyli | Yksittäinen joukkovelkakirjalaina | C 55 H 72 O 5 N 4 Mg |
| Klorofylli b | -CH 3 | -CH = CH 2 | –CHO | CH 2 CH 3 | CH 2 CH 2 COO-fytyyli | Yksittäinen joukkovelkakirjalaina | C 55 H 70 O 6 N 4 Mg | |
| Klorofylli c 1 | -CH 3 | -CH = CH 2 | -CH 3 | CH 2 CH 3 | -CH = CHCOOH | Kaksoissidos | C 35 H 30 O 5 N 4 Mg | |
| Klorofylli c 2 | -CH 3 | -CH = CH 2 | -CH 3 | -CH = CH 2 | -CH = CHCOOH | Kaksoissidos | C 35 H 28 O 5 N 4 Mg | |
| Klorofylli d | -CH 3 | –CHO | -CH 3 | CH 2 CH 3 | CH 2 CH 2 COO-fytyyli | Yksittäinen joukkovelkakirjalaina | C 54 H 70 O 6 N 4 Mg | |
| Klorofylli f | –CHO | -CH = CH 2 | -CH 3 | CH 2 CH 3 | CH 2 CH 2 COO-fytyyli | Yksittäinen joukkovelkakirjalaina | C 55 H 70 O 6 N 4 Mg |
Hapettomien fototrofien kemiallinen rakenne: bakterioklorofyylit (Bchl)
: o kaksoissidos C7 ja C8 (merkitty väri kuvassa)
b : BChl c , d ja e ovat isomeerien seos, joissa radikaali R 3 tai R 4 on eri tavalla substituoitu.
Spektriset ominaisuudet
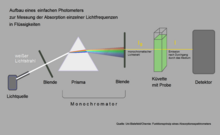
Yksinkertaista absorptiospektrometriä voidaan käyttää mittaamaan, mikä valo klorofylli absorboi erityisen voimakkaasti. Tässä esimerkissä aukko sijoitetaan siten, että keltainen valo putoaa kyvettiin klorofylli- liuoksen kanssa. Kyvetin toiselle puolelle tulevan keltaisen valon määrä tuskin laskeutuu tulevan valon määrän alapuolelle, koska klorofylli absorboi tuskin mitään näiden aallonpituuksien alueella. Jos liikutat kalvoa niin, että punainen tai sininen valo tunkeutuu, kyvetin takana oleva ilmaisin mittaa huomattavasti vähemmän päästöjä.
Absorptiospektrit in liuottimissa liuotettiin klorofyllien aina oltava kaksi erillistä absorptiomaksimit välillä 600 ja 800 nm, kuten Q y - nauha on tarkoitettu, ja toinen 400 nm, Soret band kutsutaan. Oikealla olevassa kuvassa esitetään nämä klorofyllin a ja b absorptiomaksimit . Lisäksi, on olemassa Q x nauha noin 580 nm, joka on polarisoitu kohtisuorassa Q y ja yleensä absorboi hyvin heikosti. Klorofylli a: lle se näkyy edelleen kuvassa, klorofylli b katoaa maan alle. Nauhojen välistä aluetta kutsutaan vihreäksi aukoksi .
Kuvan spektrien avulla on helppo ymmärtää, miksi klorofylliä a ja b sisältävät lehdet ovat vihreitä. Klorofylli a ja b absorboivat yhdessä pääasiassa sinisellä spektrialueella (400–500 nm) ja punaisella spektrialueella (600–700 nm). Vihreällä alueella ei sitä vastoin ole imeytymistä, joten vihreä valo hajaantuu, mikä saa lehdet näyttämään vihreiltä.
Imeytyminen riippuu liuottimesta ja vastaavasti absorptiomaksimien sijainti voi vaihdella muutamalla nanometrillä liuottimen tyypistä riippuen. Klorofylylien luonnollisessa ympäristössä eli proteiiniympäristössä asiat ovat erilaiset. Tässä absorbtiomaksimien sijainti riippuu kahdesta tekijästä: (1) Ympäröivien aminohappojen osavarauksesta ja klorofyllimolekyylien sivuryhmien taipumisesta riippuen absorptiomaksimit voivat olla hyvin erilaisia aallonpituuksia. (2) Proteiineissa klorofyylit tulevat hyvin lähelle toisiaan, joten ne ovat vuorovaikutuksessa toistensa kanssa ( dipoli-dipoli-vuorovaikutus ; hyvin lyhyillä etäisyyksillä myös vaihtaa vuorovaikutusta ). Tämä vuorovaikutus johtaa energiatason laskuun ja siten absorptiomaksimien punaiseen muutokseen. Tämä näkyy erityisen vaikuttavasti purppurabakteerien antennikompleksin LH2 esimerkissä . LH2-kompleksi koostuu kahdesta ryhmästä bakterioklorofylli-molekyylejä, jotka on järjestetty renkaaseen (katso kuva vasemmalla). Ylempi rengas (B850) sisältää 18 BChl molekyylejä, jotka ovat hyvin lähekkäin toisistaan, toisin sanoen voimakkaasti kytketty. Alempi rengas (B800) koostuu 9 BChl molekyylejä, jotka ovat huomattavasti kauempana toisistaan, ja ovat siksi paljon heikommin kytketty.
Vahva kytkentä siirtää BChl a : n imeytymisen B850-renkaassa punaiseksi. Absorptiokaista on aallonpituudella 850 nm. Heikosti kytketty BChl a B800 rengas, toisaalta, absorboivat 800 nm: ssä, eli suunnilleen samaa luokkaa kuin BChl molekyylit liuotetaan liuottimeen . LH2-kompleksin absorptiospektrissä (kuva oikealla) B800- ja B850-BChl- a- molekyylien absorptiokaistat erotetaan selvästi. Lisäksi esitetään karotenoidimolekyyleistä peräisin olevat juovat ; niitä ei ole esitetty rakenteessa.
Tyypit
On olemassa useita klorofyllityyppejä, jotka eroavat porfyriinin sivuryhmistä. Niillä on erilaiset absorptiospektrit ja niitä esiintyy eri fototrofisissa organismeissa:
| Klorofyllityyppi | väri | Absorptiomaksimit (nm) |
Tapahtuma |
|---|---|---|---|
| Klorofylli a | sinivihreä | 430, 662 (asetonissa) | Syanobakteerit ja kaikki fototrofiset eukaryootit |
| Klorofylli b | keltainen-vihreä | 454, 643 (dietyylieetterissä) | Vihreät levät ( Chlorophyta ), Euglenozoa ja kaikki maakasvit |
| Klorofylli c | vihreä | 444, 576, 626 | sen sijaan klorofylli b on ruskolevät ( Phaeophyta ), piilevät ( Bacillariophyta ), kultainen levät ( Chrysophyta ), keltainen-vihreä levät ( Xanthophyta ), tarttumalevät , Dinophyta ja Raphidophyceae |
| Klorofylli d | 447, 688 | sen sijaan klorofylli b on punalevää ( Rhodophyta ) | |
| Bakterioklorofylli a | vihreä | 358, 577, 773 (asetonissa) | Purppurabakteerit ( Rhodospirillaceae , Chromatiaceae ) |
| Bakterioklorofylli b | 368, 580, 794 (asetonissa) | Violetit rikkibakteerit ( Chromatiaceae ); Violetit bakteerit | |
| Bakterioklorofylli c | vihreä | 432, 660 (asetonissa?) | Vihreät rikkibakteerit ( Chlorobiaceae ) |
| Bakterioklorofylli c s | 740 ( in vivo ) | Vihreät rikkiä sisältämättömät bakteerit ( Chloroflexaceae ) | |
| Bakterioklorofylli d | 458, 646 (missä?) 427, 654 (asetonissa) | Vihreät rikkibakteerit ( Chlorobiaceae ) | |
| Bakterioklorofylli e | 424, 654 (missä?) 462, 649 (asetonissa) | Vihreät rikkibakteerit ( Chlorobiaceae ) | |
| Bakterioklorofylli g | 408, 418, 470, 575, 763 (missä?) 412, 788 ( in vivo ) | Heliobakteerit |
biosynteesi
Klorofylli on eukaryooteissa että kloroplastit syntetisoitu prokaryooteissa että sytoplasmassa . Monien fototrofien tapauksessa klorofyllin muodostuminen johtuu valosta, eikä sitä tapahdu ilman altistumista. Biosynteesi koostuu joukosta lukuisia vaiheita, joissa on vastaava määrä spesifisiä entsyymejä .
Tämän ja muiden tetrapyrrolien synteesi on monivaiheinen prosessi, jolla on myös erilaisia haarautumispisteitä. Biosynteesi alkaa L - glutamaatista ja päättyy siroheme -, hem - ja klorofyllihaaraan.
Usean vaiheen jälkeen uroporfyrinogeeni III muodostuu L- glutamaatista , ensimmäisestä haarautumispisteestä, josta siroheme voidaan muodostaa. Uroporfyrinogeeni III muutetaan sitten protoporfyriini IX : ksi kolmessa vaiheessa , mikä on hemin toinen haaroituspiste. In protoporfyriini IX, magnesium-ioni käyttöön ATP-riippuva reaktio, joka katalysoi magnesium chelatase ( EY 6.6.1.1 ). Tällä tavoin muodostunut Mg-protoporfyriini IX muutetaan vinyyliprotoklorofyllidiksi a Mg-protoporfyriini IX -monoetyyliesterin kautta . Tätä vaihetta katalysoi syklaasi, joka tuo viidennen renkaan klorofylliin. Kasveissa, tämä entsyymi on O 2 : sta riippuvaista, kun taas prokaryootit on sekä O 2 : sta riippuvaista ja riippumattaman cyclases.
Seuraavassa vaiheessa protokloropyllin D-rengas pelkistetään oksidoreduktaasilla divinyyliklorofylidiksi a ( EC 1.3.1.33 ) . In koppisiemenisistä tämä reaktio on täysin valoa riippuvainen. Siksi taimet eivät muodosta klorofylliä ennen kuin ne ovat alttiina valolle. Muilla kasveilla (jotkut voimistelusolut ), levillä, mutta myös syanobakteereilla on sekä valosta riippuvainen että valosta riippumaton oksidoreduktaasi. Tämän seurauksena nämä organismit voivat syntetisoida klorofylliä jopa pimeässä. Divinyyli- chlorophylid a: alennetaan ja monovinyyli- chlorophylid jonka reduktaasin ennen tämän on esteröity on klorofylli viimeisessä vaiheessa käyttäen phytol fosfaatti . Tätä terminaalivaihetta katalysoi klorofyllisyntaasi, prenyylitransferaasi ( EC 2.5.1.62 ).
Klorofylli b voidaan muodostaa myös klorofylli a: sta tai päinvastoin.
Jakautuminen klorofyllin lehtipuiden tuottaa ominainen väri lähtee syksyllä. Klorofylli on metaboloituu että klorofyllidi jonka klorofyllaasi . Tämän jälkeen suoritetaan ioninvaihto, jonka Mg 2+ - Dechelatase ja feoforbidin . Feoforbidin on hapetetaan , että feoforbidin oksygenaasin kanssa kofaktorin ferredoksiini , jolloin vihreä väri häviää ja ensimmäinen eri fluoresoiva hajoamistuotteita (FCC, mistä Englanti fluoresoiva klorofylli kataboliittien ) ja hajotetaan edelleen ei- fluoresoivat aineet (NCC) syntyy. In Maple klorofylli on toinen polku Dioxobilan purkaa.
Tärkeys fotosynteesissä
Klorofyllejä on useita tehtäviä sisällä fotosynteesi vuonna fotosysteemi I ja fotosysteemi II . Ylivoimaisesti suurin osuus käytetään valon absorbointiin ja absorboidun energian siirtämiseen. Joten ne toimivat valoherkistiminä . Tätä tarkoitusta varten klorofyllimolekyylit on järjestetty valoa kerääviin komplekseihin , jotka on järjestetty siten, että toisaalta muodostuu suurin mahdollinen absorboiva pinta ja toisaalta syntyy energinen suppilo, joka ohjaa absorboituneen energian niin kutsuttu reaktiokeskus . Reaktiossa keskustassa, kaksi klorofyllien toimivat akseptoreiden tätä energiaa. Ne on järjestetty niin, että niiden viritys johtaa varausten erottumiseen, jota voidaan pitää varsinaisen fotosynteesin ensimmäisenä askeleena. Tätä klorofylliparia kutsutaan englanniksi erityiseksi pariksi .
Valonkorjuukompleksien rakenteessa on monia eroja hyvin erilaisissa organismeissa, jotka ajavat fotosynteesiä, mutta reaktiokeskus on rakennettu melkein aina samalla tavalla. In kasvit, levät ja syanobakteerit, erityinen pari on aina muodostettu klorofylli , bakteereissa eri bakterioklorofyllien.
Esiintyminen ruoassa
Klorofyllipitoisuus on erityisen suuri vihreissä vihanneksissa. Vihannesten ja hedelmien klorofylli a- ja b- pitoisuus 100 grammassa tuoretta ainetta on lueteltu seuraavassa taulukossa klorofylli a- pitoisuuden alenevassa järjestyksessä :
| Klorofylli a | Klorofylli b | |
|---|---|---|
| Lehtikaali | 189 mg | 41 mg |
| Iso nokkonen | 185 mg | 173 mg |
| persilja | 157 mg | 55 mg |
| pinaatti | 95 mg | 20 mg |
| Parsakaali | 26 mg | 6 mg |
| vihreät pavut | 12 mg | 4 mg |
| vihreät herneet | 10 mg | 2 mg |
| kurkku | 6 mg | 2 mg |
| kiivi | 1,7 mg | 0,4 mg |
| valkokaali | 0,3-1 mg | 0,1-0,2 mg |
E 140 -merkinnällä klorofyylit ( CI Natural Green 3 ) hyväksytään elintarvikeväreinä .
Yhä useammat tutkimukset osoittavat, että sekundaarisilla kasviaineilla on positiivinen vaikutus ihmisen aineenvaihduntaan. Tämä koskee sekä klorofylliä että flavonoideja ja karotenoideja .
historia
Ensimmäiset kuvaukset etanolilla (“viinistä tislatulla alkoholilla”) uutettavalla ja valon vaikutuksesta hajoavalla ” väriaineella ” ovat Heinrich Friedrich Linkin kirjassa ”Kasvien anatomian ja fysiologian perusopetukset”, Göttingen 1807. ovat myös moniselitteisiä Todisteet siitä, että Joseph Louis Proust kuvasi vihreää väriainetta "Fécule". Pierre Joseph Pelletier ja Joseph Bienaimé Caventou uuttoivat aineen uudelleen ja nimeivät sen klorofylliksi . Ensimmäiset tutkimukset klorofyllin kemiallisesta rakenteesta ovat peräisin Richard Willstätteriltä (1913). Kemisti Hans Fischer aloitti Willstätterin tutkimuksen 1930-luvulla, ja vuonna 1940 hän pystyi selvittämään molekyylin rakenteen. Fischerin tutkimus vahvistettiin vuonna 1960 Robert B.Woodwardin klorofyllisynteesillä. Jo ennen Woodwardia ryhmä synteesiä onnistui hiukan eri tavalla Fischerin entisen työpaikan, Münchenin teknillisen yliopiston, kemikaaleilla. Fischerin entiset työntekijät Alfred Treibs ja Martin Strell jatkoivat siellä työskentelyään klorofyllin täydellisessä synteesissä. Molempien ryhmien tavoitteena oli feoforbidi a: n synteesi , koska Willstätter oli jo kuvannut jäännössynteesin tämän perusteella.
sekalaiset
Klorofyllin tärkeä ominaisuus on klorofyllin fluoresenssi . Sitä käytetään pääasiassa klorofyllipitoisuuden ja sen aktiivisuuden määrittämiseen sekä muihin tieteellisiin analyyseihin.
Hajua neutraloivan vaikutuksensa vuoksi klorofylliä on saatavana myös tabletteina apteekeissa pahanhajuisen hengityksen ja kehon hajun korjaamiseksi.
Katso myös
kirjallisuus
- Hans W.Heldt ja Birgit Piechulla: Kasvien biokemia . 4. painos. Spectrum Academic Publishing House, 2008, ISBN 978-3-8274-1961-3 .
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biokemia . 6. painos. Spectrum Academic Publishing House, Heidelberg 2007, ISBN 978-3-8274-1800-5 .
- R. Tanaka, A. Tanaka: Tetrapyrrolibiosynteesi korkeammissa kasveissa . Julkaisussa: Annu Rev Plant Biol . 58; 321-346; PMID 17227226 . 2007; doi: 10.1146 / annurev. plant. 57.032905.105448
nettilinkit
- Metabolinen reitti klorofyllin ja hemin muodostumiseen KEGG-entsyymeissä
- Absorptiospektrit Oregonin terveys- ja tiedeyliopistosta
Yksittäiset todisteet
- ^ Andreas Bresinsky, Christian Körner, Joachim W.Kadereit, G.Neuhaus ja Uwe Sonnewald: Strasburger - Kasvitieteen oppikirja . 36. painos. Spektrum Akademischer Verlag, Heidelberg 2008, s. 315, ISBN 978-3-8274-1455-7 ; S. 277.
- ^ Ian Fleming : Klorofyllin absoluuttinen kokoonpano ja rakenne , Nature 1967, 216 , 151-152 doi: 10.1038 / 216151a0 .
- Per Hyperfysiikka: Spektrivärit
- ^ Hugo Scheer (toimittaja): Chlorophylls. CRC Press, 1991. ISBN 0-8493-6842-1 .
- ↑ b c d Gerhard G. Habermehl , Peter E. Hammann, Hans C. Krebs, W. Ternes: Naturstoffchemie. Johdanto . 3. painos. Springer, Berliini 2008, ISBN 978-3-540-73732-2 , s. 530 .
- B a b c d e f g h Michael T. Madigan, John M. Martinko: Brock - mikrobiologia . 11. painos. Pearson Studium, München / Boston et ai. 2009, ISBN 978-3-8273-7358-8 , s. 607 (englanti: Brock biology of microorganisms. Kääntäjä Thomas Lazar, Freya Thomm-Reitz).
- ↑ Samuel I. Beale: Klorofyllibiosynteesin entsyymit (katsausartikkeli). Julkaisussa: Photosynthesis Research . Vuosikerta 60, 1999. sivut 43-73. Biosynteesireitti on myös esitetty tässä.
- ↑ Hans W.Heldt ja Birgit Piechulla: Kasvien biokemia . 4. painos. Spektrum Akademischer Verlag, 2008, ISBN 978-3-8274-1961-3 , s.292 .
- ^ A b T. Müller, M. Rafelsberger, C. Vergeiner, B. Kräutler: Dioksobilaani klorofyllin hajoamisprosessin tuloksena Norjassa vaahterassa. Julkaisussa: Angewandte Chemie. Osa 50, numero 45, marraskuu 2011, s. 10724-10727, doi : 10.1002 / anie.201103934 , PMID 21928453 , PMC 3262146 (ilmainen kokoteksti).
- ↑ b c P. Matile, S. Hortensteiner, H. Thomas, B. Krautler: klorofylli jakautuminen senescent lehdet. Julkaisussa: Kasvien fysiologia. Osa 112, numero 4, joulukuu 1996, s. 1403-1409, PMID 12226455 , PMC 158071 (vapaa kokoteksti).
- ↑ Merkintä E 140: Klorofyylit ja klorofylliinit Euroopan elintarvikelisäaineiden tietokantaan, käytetty 16. kesäkuuta 2020.
- ↑ Sallittujen elintarvikelisäaineiden eritelmät
- ↑ Fytokemikaalit ja niiden vaikutukset terveyteen - päivitys, joka perustuu vuoden 2012 ravintoraporttiin. Pääsy 15. huhtikuuta 2021 .
- ↑ Pelletier & Caventou, Sur la Matiere verte des Feuilles Annales de Chimie et de Physique , 1818, 9, 194–196 ( rajoitettu esikatselu Google- teoshaulla ).
- ↑ M. Strell, A. Kalojanoff, H. Koller, osittainen synteesi perusrakenteen klorofylli a, feoforbidin , Angew. Chem., 72, 169 - 170 (1960).
- ↑ Eric Fontain, Münchenin klorofyllisynteesi , TU München, 2000