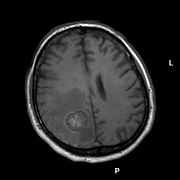
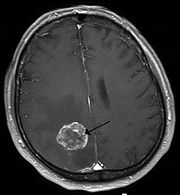
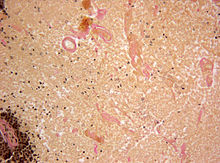
Aivojen etäpesäkkeet
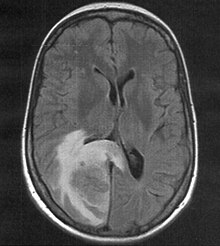
MRI T2-tunnelmapainotuksella, siihen liittyvä PET-tutkimus on esitetty alla.
| Luokitus ICD-10: n mukaan | |
|---|---|
| C79.3 | Aivojen ja aivokalvojen toissijainen pahanlaatuinen kasvain |
| ICD-10 verkossa (WHO-versio 2019) | |
Aivometastaasi on ratkaisu syöpäsolujen (etäpesäke) aivokudoksessa, jotka ovat lähtöisin pahanlaatuisten kasvainten ulkopuolella aivoihin . Termit aivot filia ( latinalaisesta filia "tytär") tai aivojen etäpesäkkeet (latina cerebralis "kuuluvat aivoihin") ovat synonyymejä .
Yleisiä alkuvaiheen kasvaimia ovat keuhkosyöpä , rintasyöpä , munuaissolukarsinooma ja pahanlaatuinen melanooma . Aivometastaasit ovat yleisimpiä pahanlaatuisten kasvainten kasvaimia, joita esiintyy aivojen alueella ja jotka voivat ilmetä muun muassa päänsärkynä, neurologisina puutoksina, kouristuksina ja persoonallisuuden muutoksina. Hoito ja toipumismahdollisuudet riippuvat monista tekijöistä, mutta aivometastaasit ovat yleensä ennusteellisesti epäedullisia olosuhteita.
Järjestelmää
- Yksinäinen aivometastaasi on läsnä, jos on olemassa yksi aivojen etäpesäke lisäksi alkuperäisestä kasvaimesta (ensisijainen kasvain) ja ei ole olemassa muita etäpesäkkeitä ulkopuolella keskushermostossa.
- Yksittäisen aivometastaasin tapauksessa toisaalta keskushermoston ulkopuolella voi olla muita metastaaseja yhden aivojen etäpesäkkeen lisäksi.
- Kaiken kaikkiaan useat eli moninkertaiset aivometastaasit ovat yleisempiä .
Kasvainsolujen kasvu keskushermoston nestetiloihin neoplastisessa meningioosissa ja harvinainen diffuusi aivokudoksen tunkeutuminen muun kuin aivokasvaimen ( karsinoosi ) kasvainsolujen kanssa on erotettava tässä hoidetuista kiinteistä aivometastaaseista .
taajuus
Luotettavaa epidemiologista tietoa aivometastaasien esiintyvyydestä saksankielisissä maissa ei ole saatavilla. Sillä Yhdysvalloissa , vuosittainen ilmaantuvuus on arvioitu noin 8,3 per 100000 väestöstä. Siellä aivometastaasit muodostavat noin puolet kaikista kliinisesti diagnosoiduista aivokasvaimista . Elämänsä aikana havaitsematta jääneiden aivometastaasien määrä on kuitenkin todennäköisesti suurempi: 1960-luvulta tehdyssä tutkimuksessa aivometastaaseja todettiin ruumiinavaus noin 1,6 prosentilla kaikista kuolleista ja noin 8 prosentissa kaikista kuolleista, joilla oli pahanlaatuisia kasvaimia keskushermoston ulkopuolella järjestelmään.
alkuperää
Yleisimmät primaarikasvaimet aivometastaaseissa ovat keuhkosyöpä (54–72%), rintasyöpä (20–34%), pahanlaatuinen melanooma ja munuaissolukarsinooma. Periaatteessa mikä tahansa pahanlaatuinen kasvain voi kuitenkin metastasoitua aivoihin. Lapsilla rabdomyosarkoomien ja sukusolukasvainten kolonisointi on vallitsevaa . Aivometastaaseja esiintyy noin 20%: lla kaikista keuhkosyöpäpotilaista, 7%: lla kaikista pahanlaatuisista melanoomapotilaisista, 7%: lla kaikista munuaissolukarsinoomapotilaista, 5%: lla kaikista rintasyöpäpotilaista ja 2%: lla kolorektaalisyöpäpotilaista.
lokalisointi
Aivometastaasien sijaitsevat pääasiassa alueella on aivoissa , mutta voi esiintyä myös pikkuaivojen ja aivorungon . Suurin osa kasvainsoluista saavuttaa aivot verenkierrossa (hematogeeninen etäpesäkkeitä). Ekstravasaatio, ts. Verisuonten poistuminen, tapahtuu arteriolaarisella tai kapillaarisella tasolla, minkä vuoksi kasvaimen kolonisaatio tapahtuu mieluiten aivokuoren ja medullaarisen kerroksen välisellä rajalla . Erityistapaus on pahanlaatuisten kasvainten etäpesäkkeitä jo olemassa olevissa hyvänlaatuisissa aivokasvaimissa.
Oireet
Aivometastaasit voivat tulla havaittaviksi ennen kuin primaarikasvaimesta tulee kliinisesti havaittavissa. Noin kolmanneksella potilaista ei tiedetä olevan kasvainta diagnoosin aikaan. Yksittäisissä tapauksissa primaarikasvain pysyy piilossa intensiivisestä hausta huolimatta ( Tuntemattoman ensisijaisen syöpä ). Toisaalta aivometastaaseja voi edelleen esiintyä vuosia syöpätaudin esiintymisen ja hoidon jälkeen (metakronisesti).
Kaiken kaikkiaan aivometastaasien oireet vastaavat pahanlaatuisten aivokasvainten, kuten glioblastooman , oireita . Koska suurin osa aivometastaaseista kasvaa nopeasti ja kudosten turvotus alueella ( perifokaalinen ödeema ) kehittyy, elinajanodote on vain muutama viikko muutamaan kuukauteen, jos sitä ei hoideta.
Yleinen mutta epäspesifinen oire on päänsärky . Syynä tähän on etäpesäkkeiden ja turvotuksen tilaa vievä vaikutus, joka voi johtaa kipuherkkien aivokalvojen venytykseen .
Muita neurologisia oireita ilmenee riippuen lokalisoinnin: jos aivot etäpesäke on alueella aivoissa, epileptisiä kohtauksia , pareses , aistien häiriöt , näkökentän puutteita tai puheen häiriöt voivat ilmetä. Persoonallisuuden ja mielialan muutokset (esimerkiksi etuosan aivosyndrooman tapauksessa ) eivät ole harvoin havaittavissa myös sivullisille. Joskus akuutti orgaaninen psykosyndrooma kehittyy paranoidilla tai aggressiivisilla piirteillä deliriumissa . Jos se sijaitsee pikkuaivojen tai aivorungon alueella, voi esiintyä huimausta , ataksiaa tai aivorungon oireyhtymiä .
Nousu kallonsisäinen paine voi aiheuttaa apatiaa , väsymys ja samentuminen tietoisuuden . Tyydyttämätön oksentelu tai kooma ovat myöhäisiä oireita, joiden ennuste on huono.
Diagnoosi
Kliininen tutkimus
Kohdennetulla neurologisella tutkimuksella on tärkeä rooli neurologisten oireiden tai valitusten tapauksessa, jotka tunnetun syövän vuoksi viittaavat aivometastaasien mahdolliseen esiintymiseen . Etsimme muun muassa merkkejä kallonsisäisestä paineesta ( kongestiivinen papilla ), kallonhermon vajaatoiminnasta ja keskushalvauksesta, jotka ovat havaittavissa lisääntyneen lihasten ja korostuneiden itserefleksien kautta, joskus myös pyramidin liikeradan merkkien kautta . Psykologiset muutokset, kokemuksen hidastuminen tai häiriöt ovat usein havaittavissa jo anamneesikeskustelussa .
Kuvantaminen
Diagnostiikan ydin on kuvantamisprosessi , jossa magneettikuvaus (MRT ) on parempi kuin tietokonetomografia (CT).
Tietokonetomografia Tietokonetomografialla
on menetelmä, joka voidaan suorittaa nopeasti ja joka on laajalti saatavilla, ja sillä on ennen kaikkea hätälääketiede . Suuremmat etäpesäkkeet eroavat normaalista aivoparenhymasta hypodenssina tai harvoin (pahanlaatuinen melanooma, korionkarsinooma ) hypertiheänä rakenteena. Koska etäpesäkkeet voivat olla myös isodenssejä , on mahdollista, että vain tilaa vievä vaikutus massansiirtona tai perifokaalisen turvotuksen hypodenssimuodostus voidaan erottaa. Keskushermoston verenvuoto, kuten sitä esiintyy erityisesti pahanlaatuisen melanooman tai munuaissolukarsinooman metastaasien yhteydessä, on helposti havaittavissa CT: ssä. Valitun kerroksen paksuudesta riippuen havaitsemisraja on noin senttimetri, jotta pienemmät etäpesäkkeet pääsevät natiivista tietokonetomografiasta. Koska tietokonetomografialla on suhteellisen alhainen pehmytkudoskontrasti, varjoaineen antaminen on ratkaisevan tärkeää: veri-aivoesteen häiriön vuoksi etäpesäkkeen alueella varjoaine kertyy (parannus) , joka on usein rengas- muotoinen tai seppeleen muotoinen , kun läsnä on keskinekroosi .
Magneettiresonanssitomografia Magneettiresonanssitomografialla
on huomattavasti suurempi herkkyys ja pehmytkudosten parempi erilaistuminen , varsinkin gadoliniumin varjoaineena antamisen jälkeen , ja on siksi sopivampi aivometastaasien etsimiseen. TT-kuvaukseen verrattuna potilaiden määrä, joilla on MRI: llä havaittuja aivometastaaseja, on yli kaksinkertainen. Tämä pätee erityisesti hyvin pieniin löydöksiin ja etäpesäkkeisiin taka-fossa-alueella. Magneettiresonanssikuvantamista voidaan käyttää erottamiseen aivojen paiseista ja muista mahdollisesti vastaavista vaurioista, jotka pakottavat täydentämään ydinmagneettisen resonanssin spektroskopiaa .

Positroniemissiotomografia positroniemissiotomografia (PET) toiminnallisena kuvantamismenetelmä (ne, Yksinkertaisesti sanottuna, metabolista aktiivisuutta kuvaannollisesti taas) mahdollistaa vastauksia tiettyihin kysymyksiin. Tällainen olisi esimerkiksi erotus hoidettavan Strahlennekrosen paikallisen uusiutumisen suhteen , ellei tätä erilaistamista voida johtaa pelkästään MRI: stä.
Angiografia
Nykyään angiografialla on vain toissijainen rooli metastaasidiagnoosissa, mutta se voi olla hyödyllinen yksittäistapauksissa kirurgisessa suunnittelussa.
CSF-diagnostiikka
Aivojen pinnalla olevien metastaasien tapauksessa kasvainsolut voivat levitä keskushermoston nestetiloihin, joka tunnetaan nimellä neoplastinen meningioosi. Että hermo nesteen ( aivo-selkäydinnesteen ) saatu mukaan lannepiston , kasvainsolut voidaan havaita, sytologian ja immunohistokemiallinen ilmentymisen profiili, joka usein avulla voidaan tehdä päätelmiä siitä, primaarikasvaimen.

Tuntemattoman primaarikasvaimen diagnoosi
Jos aivometastaaseja havaittaessa ei tunneta taustalla olevaa syöpää, ensimmäinen asia on löytää ensisijainen kasvain. Tutkimisen Ohjelma sisältää perusteellisen selvityksen ihon An X-ray rinnassa , sonography ja / tai tietokonetomografiaa rintakehän vatsan ja lantion, vuonna naisille gynekologinen tutkimus ja mammografia , ja jos on perusteltua aihetta epäillä, eli bronkoskopia kanssa bronkoalveolaariset , mahdollisesti myös positroniemissio- -Tomography tai luuston gammakuvaus . Laboratoriotutkimukset kohonneiden kasvainmerkkien suhteen ovat melko epäspesifisiä eivätkä yleensä auta.
Jos primaarikasvainta ei löydy, kudosnäyte voidaan poistaa kirurgisesti diagnoosin vahvistamiseksi, mikä tehdään yleensä stereotaktisen biopsian avulla . Kun kuolleisuus on alle 1%, histologinen diagnoosi voidaan tehdä jopa 96 prosentissa tapauksista .
Differentiaalidiagnostiikka
Pahanlaatuisten aivokasvainten ja lymfoomien lisäksi myös aivojen tulehdussairaudet, joiden kliininen kuva ja kuvantaminen voi olla samanlainen kuin aivometastaasien, tulisi ottaa huomioon differentiaalidiagnoosissa . Ei ole harvinaista, että toksoplasmoosissa esiintyviä tulehduspisteitä tai demyelinoivien yksinäisten tulehduskeskusten leikkausta kliinisellä epäilyllä aivojen etäpesäkkeistä. Septinen-embolinen aivojen paise , jota voi esiintyä hematogeenisen leviämisen yhteydessä tulehduksellisesta kohdasta (esimerkiksi tartunnan saanut sydänventtiili endokardiitissa ), on joskus vaikea erottaa metastaaseista. Hyvänlaatuiset aivokasvaimet, kuten meningiomat , jotka löydetään sattumalta kasvaimen lavastuksen aikana, on myös eroteltava.
Jos lisäkuvantaminen (magneettikuvaus, spektroskopia) ja lisätutkimukset (aivo-selkäydinnesteen poisto) eivät selvitä asiaa, tässä on ilmoitettava myös biopsia.
patologia

Neuropatologinen tarkastelu kirurginen saadun materiaalin stereotaktisella biopsialla tai resektio toimii vahvistaa diagnoosin ja sulkea muut sairaudet, joiden kliiniset ja radiologiset kuva on samanlainen kuin aivojen etäpesäke. Koska aivometastaasit voivat myös tuntea itsensä ensisijaisesti aivoverenvuotona, aivoverenvuodon neurokirurgisen poiston aikana saatu materiaali tutkitaan aina kasvainkomponenttien läsnäolon varalta.
Histologia histologia etäpesäkkeistä aivoissa muistuttaa usein, että primaarisen kasvaimen ja voi siten tarjota ensimmäinen vihjeitä niiden alkuperästä. Aivometastaasien ominaispiirre on tuumorin suhteellisen selkeä rajaaminen ympäröivästä aivokudoksesta, johon tuumori tunkeutuu kartion muodossa.
Immunohistokemia
Erityisesti silloin, kun aivojen etäpesäkkeet ovat toistaiseksi ainoa tunnistettavissa oleva syövän ilmenemismuoto, immunohistokemialliset tutkimukset voivat tarjota arvokasta tietoa primaarikasvaimen lokalisoinnista. Tässä tutkitaan proteiinien ilmentymismalleja, jotka ovat suhteellisen tyypillisiä eri primaarikasvaimille.

Esimerkiksi adenokarsinoomien aivometastaaseissa käytetään immunohistokemiallisten markkereiden ryhmää, joka sisältää sytokeratiinin alatyypit CK7 ja CK20 , kilpirauhasen transkriptiotekijä 1 (TTF1) ja prolaktiinin indusoiman proteiinin (PIP, GCDFP-15).
Metastaasien tapauksessa pahanlaatuisista melanoomista, joissa ei ole melaniinipigmenttiä , niiden melanosomaalinen erilaistuminen voidaan havaita värjäämällä melanosomaalisille antigeeneille (melanA ja HMB45).
| Ensisijainen kasvain | Ilmaisuprofiili |
|---|---|
| Keuhkosyöpä | CK7 +, CK20–, TTF1 +, GCDFP15–, melanosomaaliset antigeenit– |
| Rintasyöpä | CK7 +, CK20–, TTF1–, GCDFP15 +, melanosomaaliset antigeenit– |
| Paksusuolen syöpä | CK7–, CK20 +, TTF1–, GCDFP15–, melanosomaaliset antigeenit– |
| Pahanlaatuinen melanooma | CK7-, CK20-, TTF1-, GCDFP15-, melanosomaaliset antigeenit + |
Hoito ja ennuste
Hoito ja ennuste liittyvät läheisesti toisiinsa, koska toisaalta ennustetekijät määräävät, mitkä hoitovaihtoehdot ovat mahdollisia, ja toisaalta hoitomenetelmän valinnalla on merkittävä vaikutus elinajanodotteeseen.
Aivometastaaseissa käytetään erilaisia terapeuttisia menetelmiä. Menetelmää käytetään muun muassa aivometastaasien ja primaarikasvainten lukumäärästä, sijainnista ja koosta. Yleinen kunto potilaan, jolla on ratkaiseva vaikutus ennusteeseen ja siten myös valinta menettelyn, on myös tärkeä. Huonossa kunnossa olevat potilaat sietävät invasiivisia toimenpiteitä, kuten aivometastaasien kirurgista poistamista, huonommin kuin hyvässä kunnossa olevat potilaat. Avulla on Karnofsky-indeksin , yleiskunto voi objektiivisoida ja verrata. Mikäli mahdollista, kirurgiset, radio- ja kemoterapeuttiset toimenpiteet yhdistetään.
Oireinen hoito
Glukokortikoidit johtavat turvotuksen regressioon ympäröivään aivokudokseen kohdistuvan paineen vähenemiseen (massavaikutus) ja siten oireiden lieventämiseen; elinajanodote kasvaa keskimäärin yhdestä kahteen kuukauteen ilman lisätoimenpiteitä. Hoito tapahtuu yleensä deksametasonilla , aluksi suhteellisen suurilla annoksilla, jopa 24 milligrammaa päivässä. Se vähenee mahdollisimman pian, koska glukokortikoidien pitkäaikainen käyttö voi johtaa Cushingin oireyhtymään . Glukokortikoidien kiireellisessä hoidossa sen diagnoosi vaikeutuu, jos lymfooma on myös mahdollinen differentiaalidiagnoosi.
Aivometastaasien oireenmukaisia epilepsiakohtauksia hoidetaan antikonvulsanteilla . Toisin kuin satunnaiset kohtaukset, pitkäaikainen hoito aloitetaan täällä ensimmäisen kohtaustapahtuman jälkeen, koska uusiutumisriski on suuri. Oireellinen hoito sisältää myös kipulääkkeiden antamisen päänsärkyyn ja antiemeettisiin lääkkeisiin pahoinvoinnin ja oksentelun yhteydessä.

leikkaus
Jos potilaan yleinen tila on riittävän hyvä, yksinäiset ja yksittäiset aivometastaasit resektoidaan kokonaan kirurgisesti, jos mahdollista . Potilaan yleinen tila, kasvainsairauden vaihe ja aivojen etäpesäkkeiden kirurginen saavutettavuus ovat välttämättömiä leikkauspäätökselle. Jos yllä olevat ehdot täyttyvät, leikkaus voidaan suorittaa myös yksittäistapauksissa kahdella tai kolmella helposti saavutettavissa olevalla etäpesäkkeellä. Pienisoluisen keuhkosyövän aivometastaaseja ei yleensä operoida, koska ne reagoivat hyvin säteilyyn ja kemoterapiaan.
Jos CSF-reitit ( vesipää ) tukkeutuvat massan muutoksen vuoksi , CSF : n tyhjentämistä sisäisen tai ulkoisen salaojituksen kautta voidaan harkita tietyissä olosuhteissa .
Radiokirurgia
Alle radiosurgery viittaa soveltamiseen korkean säteilyn yhden annoksen perkutaanisesti (ihon läpi) ja stereotaktisesti sovelletaan. Se voi olla vaihtoehto tavanomaiselle leikkaukselle, jonka etäisyys etäisyydestä on kolme senttimetriä, ja sitä käytetään myös potilaille, jotka eivät ole toimintakykyisiä huonon yleisen tilan tai etäpesäkkeen sijainnin vuoksi (esimerkiksi aivorungossa). Hoidettujen etäpesäkkeiden koosta riippuen 15 - 24 harmaata annosta siedetään.
Koko aivosäteily
Koko aivojen sädehoito on tärkeä hoitovaihtoehto osana hoito-ohjelmaa etäpesäkkeistä aivoissa. Säteily on yleensä fraktioitu , ts. Useina yksittäisinä annoksina, joiden kokonaisannos on 30 - 45 harmaata, ja se peittää koko aivot, mukaan lukien kallon pohja ja kaksi ensimmäistä kohdunkaulan nikamaa. Yksittäisissä tapauksissa aivometastaasien täydellinen katoaminen voitaisiin saavuttaa. Koko aivojen säteilyä voidaan käyttää adjuvanttiterapiana täydentämään muita hoitomuotoja, jotka ovat ainoa terapian muoto tai joita voidaan käyttää myös ennaltaehkäisevästi .
Kun kyseessä on yksinäinen tai yksittäinen aivometastaasien, koko-aivot säteilytys voidaan suorittaa adjuvantly kirurgisen poiston jälkeen aivojen etäpesäkkeitä tai stereotaktinen radiosurgery. Satunnaistetuissa tutkimuksissa tutkitaan parhaillaan, tarjoaako koko aivojen lisäsäteily selviytymisen edun verrattuna pelkkään leikkaukseen. Useiden metastaasien läsnä ollessa koko aivojen säteilytystä voidaan käyttää leikkauksen lisäksi tai ainoana hoitomuotona. Profylaktinen kokoaivojen säteilytys voi vähentää oireenmukaisten aivometastaasien esiintymistä potilailla, joilla on pienisoluinen keuhkosyöpä, ja pidentää selviytymisaikaa edes pitkälle edenneessä taudissa.
Koko aivojen säteilytys voi johtaa erilaisiin sivuvaikutuksiin ja komplikaatioihin, kuten turvotuksen muodostumiseen. Erityisesti suurempien etäpesäkkeiden tapauksessa on olemassa vakavien neurologisten puutteiden riski, koska ödeeman paine naapurirakenteisiin johtuu. Glukokortikoidien anto voi vähentää turvotuksen laajuutta ja siten sivuvaikutuksia.
kemoterapia
Suurin osa aivoissa metastasoituneista kasvaimista ei ole kovin herkkä kemoterapialle, ja siksi sillä on vain vähäinen rooli aivometastaasien hoidossa. Tärkeitä poikkeuksia tähän ovat pienisoluinen keuhkosyöpä, rintasyöpä, korioninen syöpä ja sukusolukasvaimet. Yleensä käytetään samoja sytotoksisia lääkkeitä, joita käytetään metastaaseihin aivojen ulkopuolella. Monilla potilailla kemoterapia tuottaa ohimenevää vastetta, mutta yleinen elämän pidentyminen on vähäistä.
ennuste
Yleinen lausunto aivometastaasien ennusteesta ei ole mahdollista, koska siihen vaikuttavat useat tekijät. Tärkeimmät ennustekijät ovat
- rajoitus jokapäiväisistä toiminnoista johtuen kasvaimen sairauden, mitattuna on Karnofskyn indeksiin ,
- potilaan ikä,
- primaarikasvaimen hallinta,
- aika primaarikasvaimen ja aivojen etäpesäkkeiden esiintymisen välillä,
- primaarikasvaimen histologia,
- myös aivometastaasien määrä, sijainti ja koko
- metastaasien esiintyminen ja laajuus aivojen ulkopuolella.
Erilaisia ennustepisteitä on kehitetty ajan mittaan, jotta toisaalta pystytään toimittamaan riittävästi tietoa lyhyessä ajassa ja toisaalta tekemään kliinisesti riittäviä hoitopäätöksiä. Näitä indeksejä (esim. GPA , DS-GPA , Lung-mol GPA ) parannetaan ja määritetään jatkuvasti ja enemmän.
Yleensä metastaattisten syöpien ei katsota olevan pysyvästi parantuvia, lukuun ottamatta joitain sukusolukasvaimia. Metastaasien kokonaisennuste aivoissa on huono. Hoitamattomana eloonjäämisajat vaihtelevat muutamasta viikosta muutamaan kuukauteen. Nopea heikkeneminen äkillisellä kuolemalla voi johtua massiivisesta verenvuodosta etäpesäkkeeseen tai akuutista aivo-selkäydinnesteen kertymisestä. Takaosan syvennyksen (pikkuaivot ja aivorungon) metastaasit johtavat loukkuun ja siten kuolemaan , vaikka koko kasvaa . Jos potilas reagoi, optimaalinen hoito antaa mahdollisuuden parantaa elämänlaatua ja pidentää eloonjäämistä yksittäisissä tapauksissa useista kuukausista useaan vuoteen.
Eläinlääketiede
Aivometastaaseja esiintyy myös eläimillä. Eläinlääketieteessä on havaittu aivometastaasien lisääntymistä 1980-luvun puolivälistä lähtien, erityisesti pienillä lemmikkieläimillä ( koirat ja kissat ) , mikä johtuu pääasiassa hienostuneista tutkimusmenetelmistä. Tuoreessa tutkimuksessa todetaan, että yli 60% kaikista aivoissa löydetyistä kasvaimista on metastaattista alkuperää. Prosentuaalisesti koiriin vaikuttaa vaikuttavan hieman useammin kuin kissoihin. Yleisimmät primaarikasvaimet ovat sarkoomat (fibro-, osteo-, kondro- ja hemangiosarkoomat). Aivojen etäpesäkkeitä karsinoomat maitorauhasen , keuhkot , nenä ja munuaiset sekä imusuonten kasvaimet myös esiintyä.
Tutkimushistoria
Aivometastaasien muodostumisen mahdollisuus on ollut tiedossa vuosisatojen ajan. Aivometastaasien merkitystä aliarvioitiin merkittävästi, erityisesti niiden esiintyvyyden suhteen 1800-luvun loppupuolelle saakka. Niiden esiintyminen arvioitiin harvinaiseksi ja epätavalliseksi. Ensimmäiset merkittävät julkaisut ovat peräisin brittiläisiltä lääkäreiltä William Richard Gowersilta ja Byrom Bramwellilta vuonna 1888. Gowers julkaisi luokituksen, jossa kallonsisäisen kasvun syyt jaettiin kuuteen luokkaan ja järjestettiin taajuuden mukaan. Aivometastaasit olivat kolmannella sijalla karsinoomien alaryhmänä. Bramwell tunnisti, että aivometastaasit voivat periaatteessa olla peräisin mistä tahansa pahanlaatuisesta kasvaimesta, mikä on edelleen kiistaton näkemys. Lisäksi Bramwell korosti aivometastaasien joita mahdollinen kasvu aivokudoksen kasvun kanssa mikro-organismien on 1882 ympäristöön ja Robert Koch ilmaantunut agar- - keskikokoinen verrattuna. Ensimmäisen kliinisen-patologisen tutkimuksen suorittivat Globus ja Selinsky vuonna 1927. He kuvasivat tyypillisiä oireita ja patologisia muutoksia, joita esiintyy aivometastaasien yhteydessä. Tieto aivometastaasien ominaisuuksista perustuu edelleen osittain näihin varhaisiin julkaisuihin, ja sitä on jatkuvasti laajennettu lukuisilla tutkimushankkeilla.
kirjallisuus
Oppikirjat
- Mitchel Berger , Michael Prados (Toim.): Neuro-onkologian oppikirja. 1. painos, Elsevier, Philadelphia 2005, ISBN 0-7216-8148-4 .
- Uwe Schlegel, Michael Weller ja Manfred Westphal: Neuro-onkologia. 2. painos, Thieme, Stuttgart 2003, ISBN 978-3-13-109062-1 .
- Wolfgang Wick ja Michael Weller: Aivometastaasit. Julkaisussa: Thomas Brandt, Johannes Dichgans ja Hans Christoph Diener (toim.): Hoito ja neurologisten sairauksien kulku. 5. painos, Kohlhammer, Stuttgart 2007, ISBN 978-3-17-019074-0 .
Ohjeet
- Saksan neurologiayhdistyksen (DGN) S2k- ohjeet aivometastaaseista ja neoplastisesta meningioosista . Julkaisussa: AWMF online (vuodesta 2014)
nettilinkit
- Ohjeet metastaaseja ja meningoosi neoplasticaa käsittelevälle neuro-onkologiselle työryhmälle (Status 2014; PDF; 245 kB)
Yksittäiset todisteet
- ^ A b Uwe Schlegel, Michael Weller, Manfred Westphal: Neuroonkologie . Thieme, Stuttgart 2003, ISBN 978-3-13-109062-1
- ↑ aivometastaasien: muuttoliike syöpäsolujen osaksi keskushermostoon , Cancer tietopalvelu Saksan Cancer Research Center (DKFZ: sta), Heidelberg. Päivitetty 5. maaliskuuta 2007. Viimeksi katsottu 4. syyskuuta 2014.
- ↑ Walker et ai.: Aivokasvainten epidemiologia: kansallinen tutkimus kallonsisäisistä kasvaimista. Julkaisussa: Neurology. Osa 35, numero 2, helmikuu 1985, sivut 219-226, ISSN 0028-3878 . PMID 3969210 .
- ↑ Jänisch et ai .: Metastaasien esiintyvyydestä ja alkuperästä keskushermostossa. Julkaisussa: German journal for neuropathy. Osa 189, numero 1, kesäkuu 1966, sivut 79-86 , ISSN 0367-004X . PMID 5982815 .
- ^ Paul: Aivometastaasit. Julkaisussa: Neuropatologia, toimittajat Pfeiffer, Schröder ja Paulus. Springer-kustantamo. 2. painos. Berliini 2002 ISBN 3-540-41333-2
- ↑ Barnholtz-Sloan et ai .: Aivometastaasien ilmaantuvuusprosentit potilailla, joille on diagnosoitu (1973-2001) Metropolitan Detroit Cancer Surveillance System -järjestelmässä. Julkaisussa: Journal of Clinical Oncology . Osa 22, numero 14, heinäkuu 2004, sivut 2865-2872, ISSN 0732-183X . doi: 10.1200 / JCO.2004.12.149 . PMID 15254054 .
- ↑ Jarrell et ai .: Metastaasit hemangioblastoomiin von Hippel-Lindau -taudissa. Julkaisussa: Journal of Neurosurgery . Osa 105, numero 2, elokuu 2006, s.256-263, ISSN 0022-3085 . doi: 10.3171 / jns.2006.105.2.256 . PMID 17219831 .
- ^ Seute et ai.: Pienisoluisen keuhkosyövän aivometastaasien havaitseminen: kuvantamistekniikan muuttamisen seuraukset (CT vs. MRI). Julkaisussa: Cancer . Osa 112, numero 8, huhtikuu 2008, s.1827-1834 , ISSN 0008-543X . doi: 10.1002 / cncr.23361 . PMID 18311784 .
- ↑ Poptani et ai.: Kallonsisäisten massavaurioiden karakterisointi in vivo protonin MR-spektroskopialla. Julkaisussa: AJNR. Amerikkalainen neuroradiologinen lehti. Nide 16, numero 8, syyskuu 1995, s. 1593-1603, ISSN 0195-6108 . PMID 7502961 .
- ↑ Chen: PET : n kliiniset sovellukset aivokasvaimissa. Julkaisussa: Journal of nucleum medicine: virallinen julkaisu, Society of Nuclear Medicine. Osa 48, numero 9, syyskuu 2007, sivut 1468-1481, ISSN 0161-5505 . doi: 10.2967 / jnumed.106.037689 . PMID 17704239 .
- ↑ Kretzschmar et ai.: Laskennallisen tomografian ja angiografian arvo supratentorialisten aivokasvainten diagnosoinnissa. Julkaisussa: Neuroradiology. Osa 16, 1978, sivut 487-490 , ISSN 0028-3940 . PMID 745745 .
- ^ WA Hall: Stereotaktisen biopsian turvallisuus ja teho kallonsisäisiin vaurioihin. Julkaisussa: Cancer. Osa 82, numero 9, toukokuu 1998, s. 1749-1755, ISSN 0008-543X . PMID 9576298 .
- ↑ Omuro et ai.: Sudenkuopat aivokasvainten diagnosoinnissa. Julkaisussa: The Lancet Neurology . Osa 5, numero 11, marraskuu 2006, s. 937-948, ISSN 1474-4422 . doi: 10.1016 / S1474-4422 (06) 70597-X . PMID 17052661 .
- ↑ JJ Kepes: Suuret fokaaliset kasvaimen kaltaiset aivojen demyelinoivat vauriot: välituote multippeliskleroosin ja akuutin levinneen enkefalomyeliitin välillä? Tutkimus 31 potilaasta. Julkaisussa: Annals of neurology. Osa 33, numero 1, tammikuu 1993, sivut 18--27 , ISSN 0364-5134 . doi: 10.1002 / ana.410330105 . PMID 8494332 .
- ↑ B. Licata, S. Turazzi: Verenvuoto aivojen kasvainten, joilla on oireellinen hematooma. Julkaisussa: Journal of neurosurgical sciences. Osa 47, numero 4, joulukuu 2003, s. 201--210 , ISSN 0390-5616 . PMID 14978474 .
- ↑ Park et ai .: Immunohistokemiallisten markkereiden paneelit auttavat määrittämään metastaattisen adenokarsinooman ensisijaiset kohdat. Julkaisussa: Archives of Pathology & Laboratory Medicine , osa 131, numero 10, lokakuu 2007, s.1561-1567 , ISSN 1543-2165 . doi : 10.1043 / 1543-2165 (2007) 131 [1561: POIMHD] 2.0.CO; 2 . PMID 17922593 .
- ↑ Drlicek et ai.: Vasta-aineiden immunohistokemiallinen paneeli tuntemattoman primaarin aivometastaasien diagnosoinnissa. Julkaisussa: Patologia, tutkimus ja käytäntö. Nide 200, numero 10, 2004, s. 727-734, ISSN 0344-0338 . doi: 10.1016 / j.prp.2004.09.002 . PMID 15648611 .
- ↑ Mazoujian et ai.: Rintojen kystisen sairauden kokonaisproteiinin (GCDFP-15) immunohistokemia. Apokriinisen epiteelin ja rintakarsinoomien merkki, jolla on apokriinisiä piirteitä. Julkaisussa: American Journal of Pathology . Osa 110, numero 2, helmikuu 1983, s. 105-112 , ISSN 0002-9440 . PMID 6130702 . PMC 1916150 (ilmainen kokoteksti).
- ↑ Wen ym.: Aivometastaasien hoito suotuisilla ennustepotilailla . UpToDate elokuu 2007.
- ↑ a b c DGN -ohjeet: Kiinteät aivometastaasit . Tila: 2008 ( online-versio )
- ↑ Drappaz et ai .: Vasogeenisen turvotuksen hoito potilailla, joilla on primaarisia ja metastaattisia aivokasvaimia . UpToDate elokuu 2007.
- ↑ J. Lokich, H. Levine, I. Nasser: pahanlaatuisuuteen liittyvä vesipää: kliiniset piirteet ja kammioperitoneaalisen shuntimenettelyn tulokset kolmella potilaalla. Julkaisussa: American Journal of Clinical Oncology . Osa 21, numero 4, elokuu 1998, sivut 366-368, ISSN 0277-3732 . PMID 9708635 .
- ↑ Astner et ai.: Aivojen sisäisten etäpesäkkeiden sädehoito. Onkologi 2008; 14: 246-254
- ↑ JG Cairncross, NL Chernik, JH Kim, JB Posner: Aivometastaasien sterilointi sädehoidolla. Julkaisussa: Neurology . Osa 29, numero 9, s. 1, syyskuu 1979, s. 1195-1202 , ISSN 0028-3878 . PMID 225696 .
- ^ Euroopan syövän tutkimus- ja hoitojärjestö: Adjuvanttinen sädehoito aivometastaaseja sairastavien potilaiden hoidossa . ClinicalTrials.gov Tunniste: NCT 00002899
- Ot Slot et ai .: Profylaktinen kraniaalinen säteilytys laajamittaisessa pienisoluisessa keuhkosyövässä. Julkaisussa: The New England journal of medicine . Osa 357, numero 7, elokuu 2007, sivut 664-672, ISSN 1533-4406 . doi: 10.1056 / NEJMoa071780 . PMID 17699816 .
- ↑ Carsten Nieder, Minesh P.Mehta: prognostiset indeksit aivometastaaseille - hyödyllisyys ja haasteet . Julkaisussa: Radiation Oncology (Lontoo, Englanti) . nauha 4 , 4. maaliskuuta 2009, ISSN 1748-717X , s. 10 , doi : 10.1186 / 1748-717X-4-10 , PMID 19261187 , PMC 2666747 (ilmainen kokoteksti) - ( nih.gov [käytetty 4. toukokuuta 2021]).
- ^ Koestner & Higgins: Keskushermoston metastaattiset kasvaimet, Pack DJ: Kasvaimet kotieläimissä. Blackwell, 2002: 737-738 ISBN 0-8138-2652-7
- ^ Raymond Sawaya: Kallonsisäiset etäpesäkkeet: Nykyiset hallintastrategiat . Wiley-Blackwell 2004, ISBN 1-4051-1646-3