Ioninen neste

Ioninesteet ( englantilaiset ioniset nesteet ( IL ), myös huoneenlämpöiset ioniset nesteet (RTIL) ) ovat suoloja, joiden sulamislämpötila on alle 100 ° C. Vakaan kidehilan muodostumista estävät varauksen delokalisointi ja steeriset vaikutukset. Jopa pieni määrä lämpöenergiaa on siis riittävä voittamaan hilaenergia ja hajottaa kiinteän kiteen rakenne.
Vaihtamalla kationia ja anionia ionisen nesteen fysikaalis-kemiallisia ominaisuuksia voidaan muuttaa laajoissa rajoissa ja optimoida teknisten vaatimusten mukaisesti. Sulamispisteen lisäksi voidaan vaikuttaa esimerkiksi homogeenisten katalyyttien , tuotteiden tai lähtöaineiden liukoisuuteen ioniseen nesteeseen.
Aromaattiset heterosyklit, kuten imidatsolium- tai pyridinium- käytetään usein , koska kationeja , jotka voidaan alkyloida . Sopivia alifaattisia yhdisteitä ovat esimerkiksi pyrrolidinium , guanidinium , uronium , tiouronium , piperidinium , morfolinium , ammonium ja fosfonium . Kuten anioneja ovat halogenidit ja heikosti koordinoivan ionit , kuten tetrafluoriboraatit , heksafluorifosfaatti tai sulfonamidit, mutta myös trifluoriasetaatit , triflaatit , fosfinaatit ja tosylaatit kyseessä.
tarina
Ionisten nesteiden lähihistoria voidaan jakaa kolmeen sukupolveen, joiden rajat ovat neste. Julkaisuja, jotka merkitsevät selvästi sukupolven alkua, löytyy vain ensimmäisestä ja toisesta sukupolvesta. Sukupolvien laskeminen alkaa vasta 1980 -luvulla, jolloin ionisia nesteitä tuotettiin ja tutkittiin erityisesti niiden ominaisuuksien perusteella. Ensimmäiset kuvaukset suoloista, jotka täyttävät ionisten nesteiden määritelmän, julkaistiin jo vuonna 1876.
Ensimmäiset kuvaukset (1876–1929)
William Ramsey kuvasi pikoliinia ja sen johdannaisia vuonna 1876 , mukaan lukien pikoliniumtribromidi ja pikoliniumtriiodidi. Se valmistetaan sekoittamalla halogeenit vastaavien pikoliniumhalogenidien kanssa. Sulamispiste on 85 ° C pikoliniumtribromidille ja 79 ° C. Mukaan alkyloiva pikoliini, edelleen ionisia nesteitä voitaisiin saada vuonna 1899. Esimerkiksi 1-propyyli-2-pikoliniumjodidille on raportoitu sulamispiste 77 ° C. Homologinen 1-butyyli-2-pikoliniumjodidi on myös ioninen neste, jonka sulamispiste on 98 ° C. Analogisen yhdisteen, jossa on isobutyyliradikaali, sulamispiste on alle -15 ° C ja on siten ensimmäinen ioninen neste, joka on nestemäinen huoneenlämpötilassa.
Toinen aine, jonka tarkka rakenne ja siten luokittelu ioniseksi nesteeksi jäi tuntemattomaksi yli 100 vuoden ajan, on ns. ”Punainen öljy”. Tämä tapahtuu sivutuotteena Friedel-Crafts-alkylaatioissa , jotka kuvattiin ensimmäisen kerran vuonna 1877. Rakenteellisesti "punainen öljy" on kationinen Wheland -välituote ja dialumiininen heptakloridianioni.
Gabrielin ja Weinerin synteesi ja kuvaus etanoliammoniumnitraatista, jonka sulamispiste oli 52 ° C, seurasi vuonna 1888.
Edellisistä kuvauksista huolimatta etyyliammoniumnitraattia (EAN) kuvataan usein kirjallisuuden ensimmäisenä ionisena nesteenä. Vuonna 1914 Paul Walden syntetisoi EAN: n, jonka sulamispiste on 12 ° C, saattamalla etyyliamiinin ja typpihapon reagoimaan . Vaikka Walden pystyi myös mittaamaan EAN: n johtavuuden, ionisten nesteiden potentiaali jäi selvittämättä. Vain yksi tutkimus joidenkin suolojen laskuvarjosta ( molaarisen tilavuuden mitta samalla pintajännityksellä ) vuodelta 1929 tutki ionisten nesteiden erityispiirteitä.
Kehitys (1950–1972)
Vuonna 1951 voitiin kuvata ionisen nesteen ensimmäinen käyttö. Hurley ja Wier sekoittivat etyylipyridiniumbromidin alumiinikloridin kanssa eri koostumusten ionisten nesteiden saamiseksi . Muuttamalla alumiinikloridin ja etyylipyridiniumbromidin sekoitussuhteita he löysivät kaksi eutektiaa : yhden suhteessa 1: 2, sulamispiste 45 ° C ja toisen suhteessa 2: 1, sulamispiste -40 ° C. 1: 1 -seos sulaa 88 ° C: ssa ja on siten myös ioninen neste. Näitä ionisia nesteitä voitaisiin käyttää alumiinin sähkökemiallisessa kerrostamisessa eri metalleille.
Vuonna 1963 Yoke kuvasi trietyyliammoniumhydrokloridin reaktion kupari (I) kloridin kanssa , mikä johti nestemäiseen tuotteeseen. Koska yhdiste ei kuitenkaan ole ilmakestävä, koska Cu (I) on hapetettu, sitä ei tutkittu tarkemmin.
Kornblum ja Coffey kuvasivat ensimmäisen ionisen nesteen, jossa oli tetrafluoriboraattianionia, vuonna 1966. Saattamalla natriumsuola 2-pyridonin kanssa trietyylioksoniumtetrafluoriboraattia , N- etyyli-2-ethoxypyridinium tetrafluoriboraatti voidaan saada joka sulaa 47,5-48,5 ° C: ssa
Ionisten nesteiden käyttö liuottimina esiteltiin ensimmäisen kerran vuonna 1972. Parshall onnistui tuottamaan kaksi tetraetyyliammoniumiin perustuvaa ionista nestettä. Triklooristartaattia ja trikloorgermanaattia käytettiin anioneina. Erityisesti tetraetyyliammoniumstannaattia voidaan käyttää liuottimena, koska se voi liuottaa jopa 7 painoprosenttia platina (II) kloridia . Tämä liuos voi toimia katalyyttisesti aktiivisena reaktioväliaineena olefiineille, jotka voidaan hydrata , hydroformyloida tai karboalkoksyloida .
Ensimmäisen sukupolven ioniset nesteet (vuodesta 1978)
Haloaluminaatit tunnetaan ensimmäisen sukupolven ionisina nesteinä. Hurley ja Wier kuvailivat niitä jo vuonna 1951, mutta ne siirtyivät tutkimuksen painopisteeseen vasta 1970 -luvulla. US Air Force Academy on tutkinut alhaisessa lämpötilassa elektrolyyttejä käytettäväksi akut, sillä 1960-luvun alussa, muun muassa yhteistyössä Robert Osteryoung. Molempien tutkimusryhmien julkaisut merkitsevät ionisten nesteiden modernin aikakauden alkua: Vuonna 1978 Osteryoung pystyi kuvailemaan ja tutkimaan alumiinikloridi: 1 -butyylipyridiniumkloridi (AlCl 3 -BPC) -järjestelmää ensimmäistä kertaa . Samana vuonna Yhdysvaltain ilmavoimat haki patenttia "AlCl3 / 1-alkyylipyridiniumkloridin huoneenlämpöiset elektrolyytit". Vaikka nämä suolat sulavat aikaisemmin kuin alumiinikloridin ja natriumkloridin seokset, joita ilmavoimat olivat aiemmin käyttäneet elektrolyytteinä, alumiinikloridin ja 1-butyylipyridiniumkloridin (1: 1) seos ei ole nestemäinen huoneenlämmössä, vaan sulaa vain 40 ° C: ssa. ° C. Toinen haitta on pyridiniumkationin kapeneva sähkökemiallinen ikkuna, jota voidaan pienentää. Wilkesin ja Husseyn ryhmä alkoi sitten etsiä sopivampaa kationia, joka on vakaa pelkistykseen verrattuna alumiiniin. He pystyivät tunnistamaan ja syntetisoimaan dialkyyli-imidatsoliumkationeja sopivina ehdokkaina käyttämällä semi-empiirisiä molekyylin kiertoradan laskelmia vuonna 1982 .
Molemmat AICI 3 -BPC ja 1-etyyli-3-metyyli-variantti voidaan käyttää ei-vesipitoiset ja polaariset liuottimet siirtymämetallikompleksit . Niin voisi z. B. Heksakloromolybdaatti (III) ja heksakloromolybdaatti (IV) anioneja tuotetaan ja tutkitaan ensimmäistä kertaa ionisissa nesteissä. Seuraavina vuosina ionisia nesteitä tutkittiin yhä enemmän katalyyttisesti aktiivisina liuottimina. Sovelluksia ovat nukleofiiliset aromaattiset substituutiot tetraalkyylifosfonium - IL - yhdisteissä tai Friedel-Crafts-alkyloinnissa ja asetyloinnissa 1-etyyli-3-metyyli-imidatsoliumtetrakloorialuminaatissa.
Toisen sukupolven ioniset nesteet (vuodesta 1992)
Kloorialuminaattipohjaisten ioninesteiden suuri haitta on niiden herkkyys vedelle. Hydrolyysin aikana muodostuu muun muassa syövyttävää suolahappoa . Alkuperäisessä sovelluksessa akkuteknologiassa herkkyys hydrolyysille ei ollut merkityksellinen, koska paristojen piti joka tapauksessa toimia ilman kosteutta, mutta käsittely laboratoriossa oli lähes yksinomaan mahdollista hansikaslokerossa . Vuonna 1990 Mike Zaworotko aloitti ilmavoimien akatemiassa ja vuonna 1992 julkaisi yhdessä Wilkesin kanssa ensimmäisen paperin ilma- ja vedenkestävistä ioninesteistä. Tämä lisääntynyt stabiilisuus voitaisiin saavuttaa vaihtamalla kloorialuminaattianioni. Tyypillisiä anioneja toisen sukupolven ioninesteissä ovat halogenidit kloridi, bromidi ja jodidi sekä tetrafluoriboraatti, heksafluorifosfaatti tai bentsoaatti. Vuonna 1996 imidatsoliumpohjaisissa ioninesteissä käytettiin ensimmäistä kertaa perfluoroituja anioneja, kuten bis (trifluorimetyylisulfonyyli) amidi, triflaatti tai trifluoriasetaatti . Näille ionisille nesteille on ominaista niiden hydrofobisuus , alhainen sulamispiste, joskus alle -30 ° C, ja korkea johtavuus.
Kolmannen sukupolven ioniset nesteet (noin 2000 tähän päivään)
Kun toisen sukupolven uudet anionit ovat laajentaneet ionisten nesteiden kenttää, kolmannen sukupolven pitäisi laajentaa spektri arviolta 10 18 mahdolliseen yhdistelmään. Tästä poolista tuotettiin ns. "Tehtäväkohtaisia ionisia nesteitä" tai "suunnitteluliuottimia" ja ne on räätälöity erityisesti tiettyihin sovelluksiin. Tämä sisältää myös kiraaliset ioniset nesteet ja "syväeutektiset liuottimet". Kolmannen sukupolven ioniset nesteet mainitaan usein "vihreän" kemian yhteydessä, koska ne ovat vaihtoehto yleisesti käytetyille haihtuville, myrkyllisille ja syttyville liuottimille.
Jo vuonna 1996 Eastman Chemical suoritti ensimmäisen suuren mittakaavan prosessin, jossa käytetään ionista nestettä.
Valmistus
Ioninesteiden synteesi tapahtuu yleensä kahdessa vaiheessa: Ensimmäisessä vaiheessa tuotetaan haluttu kationi, yleensä kvaternointireaktion avulla, ja toisessa vaiheessa seuraa anionimetateesi.
Kvaternisaatio
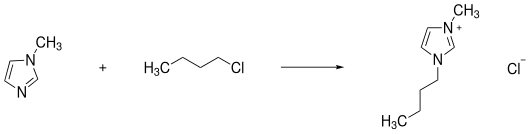
Kvaternisointireaktio on nukleofiilinen substituutio. Alkylointiaine, tavallisesti halogeenialkaani, saatetaan reagoimaan typpeä sisältävän heteroaromaattisen aineen, kuten pyridiini- tai imidatsolijohdannaisten kanssa. Menetelmää voidaan käyttää myös muille riittävän nukleofiilisille aineille, kuten amiineille. Jos alkylointiaineen poistuva ryhmä on jo haluttu anioni, ionisten nesteiden synteesi on jo saatu päätökseen. Tämä on erityisen tärkeää ionien nesteiden halogenidittomassa synteesissä. Dimetyyli ja dietyylisulfaatti voivat toimia alkylointiaineina . Lisäksi esimerkkejä, joissa ioniset nesteet saadaan kvaternointireaktio ovat alkylointeja metyylitriflaattia tai synteesiä [bmim] Cl päässä metyyli- ja klooributaanista .
Anionin metateesi
Halutun anionin saamiseksi on periaatteessa kolme tapaa vaihtaa anioni:
Kun metalli- tai ammoniumsuola M + [A] - reagoi , ionisten nesteiden ja tuloksena olevan ei -toivotun suolan liukoisuuskäyttäytyminen hyödynnetään. Joko tämä saostuu suoraan liuottimesta, kuten monien hopeasuolojen tapauksessa, tai käytetään kaksifaasisia seoksia.
Metallisuolan sijasta voidaan käyttää myös anionin Brønsted -happoa . Tämän menetelmän etuna on, että puhdistus on helppoa haihduttamalla ei -toivotun anionin happo.
Kolmas vaihtoehto on käyttää vaihtohartsia .
Lewisin hapot
Toinen lähestymistapa on antaa anionin reagoida Lewisin hapon kanssa. Esimerkiksi kloridisuola voidaan sekoittaa alumiinitrikloridin kanssa. Tetrakloorialuminaatti muodostuu sitten in situ .
Tätä menetelmää käytetään ensimmäisen sukupolven ioninesteiden synteesiin.
Protiset ioniset nesteet
Protoonisia ionisia nesteitä voidaan tuottaa happo-emäs-reaktiolla . Tämä on tasapainoreaktio, joka riippuu hapon tai emäksen vahvuudesta.
- Happo + emäs on tasapainossa konjugaatin (vastaava) emäs + konjugaatti (vastaava) hapon kanssa
Tasapainoreaktion vuoksi monilla proottisilla ionisilla nesteillä on asianmukainen höyrynpaine ja ne voidaan puhdistaa tislaamalla. Esimerkki tertiääriseen amiiniin perustuvasta proottisesta ionisesta nesteestä on etyyliammoniumnitraatti.
ominaisuudet
| ominaisuus | orgaaninen liuotin | ioninen neste |
| määrä | > 1000 | > 10 6 |
| prosessikohtainen toiminto | yksitoiminen | monitoiminen |
| kustannuksia | pieni määrä | 2–100 kertaa korkeampi kuin org. liuotin |
| Höyrynpaine | on höyrynpaine (VOC) | ei merkittävää höyrynpainetta |
| Syttyvyys | enimmäkseen syttyvää | ei syttyvää |
| sopeutumiskyky | rajoitettu määrä | suunnitteluliuottimet |
| Kiraalisuus | Harvinainen | yleinen ja muokattavissa |
| Katalyyttinen aktiivisuus | Harvinainen | yleinen ja muokattavissa |
| Viskositeetti [mPas] | 0,2-100 | 20-97000 |
| Tiheys [g · cm −3 ] | 0,6-1,7 | 0,8--3,3 |
| sähkönjohtavuus [mS · cm −1 ] | lähinnä eristimiä | 120: een |
| lämmönjohtavuus [W · m −1 · K −1 ] | 0,1-0,6 | 0,1-0,3 |
Ioninesteille on ominaista useita mielenkiintoisia ominaisuuksia. Mahdollisuuksien suuren määrän vuoksi ominaisuudet voidaan kuitenkin tiivistää vain osittain ja jotkut ioniset nesteet eroavat huomattavasti toisistaan. Useimmat ioniset nesteet ovat verrattain lämpöstabiileja, vaikeita syttyä, niiden höyrynpaine on erittäin alhainen, tuskin mitattavissa ja niillä on erittäin hyvät liukoisuusominaisuudet useille aineille. Puhtaasti ionisen rakenteensa vuoksi niillä on myös mielenkiintoisia sähkökemiallisia ominaisuuksia, kuten B. sähkönjohtavuus, johon usein liittyy korkea sähkökemiallinen stabiilisuus hapettumista ja pelkistymistä vastaan. Ionien välisiä sähköstaattisia vuorovaikutuksia voidaan kuvata Poisson-Boltzmannin yhtälöllä . Vertailu perinteisiin orgaanisiin liuottimiin osoittaa joitakin ionisten nesteiden erityisominaisuuksia ja ratkaisevia eroja. Yksi ominaisuuksista, jotka ovat ratkaisevia ionisten nesteiden käyttämisessä liuottimina, on alhainen, yleensä vähäinen höyrynpaine. Vaikka VOC -yhdisteet ovat ympäristö- ja työturvallisuusongelma, ioniset nesteet ovat tältä osin vaarattomia ja niitä voidaan käyttää jopa avaruussovelluksiin. Poikkeuksena ovat proottiset ioniset nesteet (PIL), joilla on korkeampi höyrynpaine happo-emästasapainon vuoksi. Syttyvyys on toinen turvallisuuteen liittyvä ominaisuus. Ioninesteet eivät yleensä ole syttyviä, vaikka tätä ominaisuutta voidaan myös muuttaa kohdennetusti, esim. B. polttoaineille. Erinomainen ominaisuus, jonka ioniset nesteet ovat tuoneet tutkimuksen kohteeksi, on sähkönjohtavuus. Vain tämän ominaisuuden vuoksi ioniset nesteet soveltuvat sähkökemiallisiin sovelluksiin, kuten energian varastointiin ja muuntamiseen. Niitä voidaan käyttää esimerkiksi akkutekniikassa ja aurinkokennoissa. Vaihtamalla kationin sivuketjuja ja valitsemalla sopivia anioneja esimerkiksi liukoisuus veteen tai orgaanisiin liuottimiin voidaan määrittää suurelta osin vapaasti. Sama koskee sulamispistettä ja viskositeettia. Ne voidaan syntetisoida hapoina , emäksinä tai ligandeina sopivien funktionaalisten ryhmien avulla . Sovelluksissa ne voivat paitsi ottaa liuottimen roolin, myös toimia katalyyttinä tai tuoda stereotietoja reaktioon.
Sulamispiste
Ionisten nesteiden määrittelevä ominaisuus on sulamispiste. Sulamispisteen tarkka määrittäminen ei useinkaan ole vähäpätöistä, koska lasisiirtymä voi tapahtua, kun ioniset nesteet jäähtyvät .
Sulamispiste määräytyy olennaisesti anionin ja kationin välisestä Coulomb -vuorovaikutuksesta. Tämä vuorovaikutus voidaan kuvata seuraavalla yhtälöllä:
Yhtälö osoittaa, että vuorovaikutuksen kokoon vaikuttavat kolme tekijää:
- Ionien varaus ja : Pienen vuorovaikutuksen ja siten alhaisen sulamispisteen vuoksi sekä anionia että kationia tulee ladata vain kerran.
- Ionien välinen etäisyys : Suuremmat ionit johtavat suurempiin etäisyyksiin ja siten alempiin sulamispisteisiin.
- Madelungin vakion antama ionien pakkaustehokkuus : Tähän vaikuttaa ionien epäsymmetria. Suurempi epäsymmetria johtaa yleensä alhaisempiin sulamispisteisiin.
Muita tekijöitä ovat van der Waalsin vuorovaikutus , π-π-vuorovaikutus ja vetysidokset .
Tästä johdetaan suuntauksia, jotka Coulombin voimiin kohdistuvien vaikutusten lisäksi auttavat ennustamaan ionisen nesteen sulamispisteen:
- korkea konformaatiojoustavuus ja kiraaliset keskukset johtavat alempaan sulamispisteeseen
- vähemmän tehokas pakkaus johtaa alempaan sulamispisteeseen
- korkea symmetria johtaa korkeampaan sulamispisteeseen
- Vetysidosten lukumäärä ja laajuus, anionit, joilla on suuri taipumus muodostaa vetysidoksia (CH 3 COO - ), sekä anionit, jotka eivät voi muodostaa vetysidoksia ([(CF 3 SO 2 ) N] - ), ovat sulavia
- funktionaaliset ryhmät, kuten B. Eetteritoiminnot johtavat alempiin sulamispisteisiin
Sähkökemiallinen ikkuna
Sähkökemiallinen ikkuna ( sähkökemiallinen ikkuna , EW) osoittaa sen alueen koon, johon aine ei hapetu eikä pelkisty. Se kuvaa eroa anodin ja katodin rajoittavien potentiaalien välillä:
Mitä suurempi on sähkökemiallinen ikkuna, sitä vakaampi aine on hapettumista ja pelkistymistä kohtaan. Ionisille nesteille on ominaista erittäin suuri sähkökemiallinen ikkuna. Kationi on enimmäkseen vastuussa katodin rajoittavasta pelkistyspotentiaalista ja anionin hapettumispotentiaalin anionista. Heptakloorialuminaattianioni Al 2 Cl 7 - on poikkeus . Tyypilliset sähkökemialliset ikkunat ovat alueella 3–6 V. Verrattuna veteen, jonka ikkuna on suhteellisen pieni, 1,2 V, ionisten etu on ilmeinen tässä Nesteet sähkökemialliset sovellukset. Esimerkiksi [BMIM] [BF 4 ]: n sähkökemiallinen ikkuna on 4,1 V, [BMIM] [PF 6 ] yksi 4,15 V: sta, kun taas [BMPyrr] [NTf 2 ] -ikkuna on 5,5 V. Erinomainen esimerkki on 1-metyyli-1-propyylipiperidiniumheksafluorifosfaatti , jonka sähkökemiallinen ikkuna on 7,2 V, jota rajoittavat katodipotentiaali -3,25 V ja anodipotentiaali 3,95 V. 100 ° C: n sulamispisteen vuoksi se kuitenkin lähes putoaa ionisen nesteen määritelmän ulkopuolelle. Jotta ionisten nesteiden suuri sähkökemiallinen ikkuna voidaan hyödyntää täysimääräisesti, on tärkeää syntetisoida ne sekä vedestä että halogeenittomasta. 3 paino-% vettä johtaa jo siihen, että [BMIM] [BF 4 ]: n sähkökemiallinen ikkuna laskee 4,1: stä 1,95 V.
käyttää
Periaatteessa ionisten nesteiden molekyylien monimuotoisuus mahdollistaa niiden käytön monilla teknisillä sovellusalueilla. Niiden käyttö laajamittaisissa prosesseissa osoittaa niiden merkityksen kemiallisten prosessien suunnittelussa ja reaktiotekniikassa . Myös bioprosessitekniikan sovelluksia tunnetaan. Yksi ionisten nesteiden tärkeimmistä käyttökohteista on elektrolyytti polttokennoissa, kondensaattoreissa, paristoissa, väriaineiden aurinkokennoissa ja metallin viimeistelyssä. Lisäksi elektrodien ja elektrolyyttien rajapintojen mallijärjestelminä. Muita sovelluksia ovat lämmönsiirto, käyttö jäähdytysaineena ja ionikompressorina sekä erityisanalyyseissä GC-päätilan ja MALDI-TOF-MS: n matriisimateriaaleina, Karl Fischer -prosessin liuottimet , väliaine proteiinien kiteyttämiseen ja elektroforeesiin . Synteesissä ioniset nesteet voivat toimia sekä katalyyttinä että liuottimena. Se kattaa orgaaniset ja epäorgaaniset synteesit sekä polymeerit ja nanohiukkaset.
elektrolyytti
Väritä aurinkokennot
Väriaurinkokennojen avulla voidaan käyttää laajempaa valospektriä verrattuna kiteisiin pii -aurinkokennoihin , mikä mahdollistaa myös hajavalon tai pienemmän valon käytön. Ionisia nesteitä voidaan käyttää uutena elektrolyyttimateriaalina. Tässä on hyötyä niiden johtavuudesta, joka takaa tarvittavan varauksen siirron. Yhdessä alhaisen sulamispisteen ja erittäin alhaisen höyrynpaineen kanssa sitä voidaan käyttää -20 - +80 ° C: n lämpötiloissa. Niillä on myös korkea sähkökemiallinen stabiilisuus. Yksi sovellus pyrkii käyttämään näitä soluja, esim. B. matkapuhelimien laturina alueilla, joilla ei ole valtakunnallista virtalähdettä.
Paristot
Monissa kaupallisissa litiumioniakkuissa on usein orgaanisia liuottimia , esim. B. käytetä karbonaatteja kuin elektrolyytti . Näillä on kuitenkin useita haittoja. Ionisiin nesteisiin verrattuna orgaanisilla karbonaattiliuottimilla on rajoittava stabiilisuus hapettumista vastaan suurilla positiivisilla potentiaaleilla (noin 4,3-4,9 V vs. Li + / Li) käytetystä elektrodista riippuen. Tämä johtaa elektrolyytin lisääntyvään hajoamiseen, kun nämä potentiaalit kiertävät asteittain. Tehokkuuden heikkenemisen vuoksi orgaaniset liuottimet sopivat vain pieneen mahdolliseen ikkunaan. Toinen etu on ionisten nesteiden terminen vakaus ja alhainen haihtuvuus. Paikallisen ylikuumenemisen tai oikosulun vuoksi elektrolyytin ja muiden akun osien välillä voi esiintyä ei -toivottuja eksotermisiä reaktioita. Nopeasti nouseva solulämpötila voi aiheuttaa orgaanisen liuottimen syttymisen. Suurin haitta ionisten nesteiden käytölle elektrolyytteinä on niiden alhainen ionijohtavuus, koska niillä on alhainen varaustiheys ja suuret steeriset esteet .
Selluloosan viimeistely
Selluloosa on määrältään suurin luonnollinen orgaaninen kemikaali maailmassa, ja sitä esiintyy noin 700 miljardia tonnia, ja sillä on suuri merkitys uusiutuvana raaka -aineena . Luonnosta vuosittain lisääntyvistä 40 miljardista tonnista vain noin 0,2 miljardia tonnia käytetään raaka -aineena jatkokäsittelyyn. Selluloosan pitkäaikainen käyttö raaka -aineena estää sopivan liuottimen puuttumisen. Robin Rogers ja kollegat Alabaman yliopistosta ovat havainneet, että ionisten nesteiden käyttö voi tuottaa selluloosan liuoksia teknisesti käyttökelpoisina pitoisuuksina. Esimerkiksi synteettisten selluloosakuitujen (esim. Viskoosin ) valmistuksessa ns. Kemiallisesta massasta on tällä hetkellä käytettävä suuria määriä apukemikaaleja, erityisesti hiilidisulfidia (CS 2 ), ja kierrätettävä tai hävitettävä. Lisäksi prosessin luonteen vuoksi on käsiteltävä huomattavia määriä jätevettä. Näitä prosesseja voidaan mahdollisesti yksinkertaistaa käyttämällä ionisia nesteitä, koska niitä voidaan käyttää liuottimina ja lähes kokonaan kierrättää. Tekstiilikemian ja tekokuitujen instituutti (ITCF) Denkendorfissa ja BASF tutkivat yhdessä niiden kuitujen ominaisuuksia, jotka kehrätään koelaitoksessa ionisten nesteiden avulla liuotetusta selluloosasta.
Selluloosan hyvä liukoisuus ionisiin nesteisiin avaa monia mahdollisuuksia uusiutuviin raaka -aineisiin perustuvien materiaalien tuottamiseen. Yksivaiheisessa synteesissä selluloosa voidaan muuntaa 5-hydroksimetyylifurfuraaliksi (HMF) kytkettyjen kupari (II) kloridi / kromi (II) kloridikatalyyttien läsnä ollessa liuottimessa 1-etyyli-3-metyyli-imidatsoliumkloridi 80-120 ° C: ssa ° C. mahdollinen rakennusmateriaali biomassaan perustuville muoville.
Lääkkeet
Yli 50% kaupallisesti saatavista lääkkeistä on suolojen muodossa. Yleensä vain yksi ioneista on luonteeltaan orgaaninen; suosituimmat vastaionit ovat natrium ja kloridi. Farmaseuttisesti aktiivisilla aineilla on yleensä funktionaalisia ryhmiä, jotka voidaan muuntaa ioneiksi. Esimerkiksi amiinit voivat muodostaa kationeja, happofunktionaalisuudet voivat muodostaa anioneja.
Tämän perusteella voidaan noudattaa kahta lähestymistapaa. Yhdistämällä kaksi farmaseuttisesti aktiivista ionia saadaan tuote, jolla on anionien ja kationien aktiivisuus. Ionien välinen synergistinen vaikutus, joka saa aikaan halutun vaikutuksen voimistumisen, on optimaalinen . Toinen lähestymistapa "nesteyttää" farmaseuttisesti aktiivisen ionin valitsemalla inertin tai biologisesti yhteensopivan vastaionin. Näin vältetään monien suolojen polymorfismin aiheuttamat ongelmat .
Lisäksi ionisia nesteitä voidaan käyttää lääkkeiden synteesissä, mutta myös liuottimina, emulgointiaineina tai lääkkeenjakelujärjestelminä .
Farmaseuttisesti aktiiviset ioninesteet ovat jo tunnettuja. Sallittuja ovat setyylipyridiniumkloridi , antiseptinen aine ja bretylium , rytmihäiriölääke .
biotekniikka
Ioninesteet laajentavat biotransformaatioiden valikoimaa, koska niissä voidaan suorittaa myös vesiherkkiä reaktioita. Roger A. Sheldon ryhmä suorittaa pioneerityö biotransformaatiotapoja ionisiin nesteisiin 2000 kautta lipase- katalysoimien reaktioiden alkoholyysin , ammonolyysi ja perhydrolyysi. Candida antarctica lipaasi B (CaLB) käytettiin ionisten nesteiden [bmim] [PF 6 ] ja [bmim] [BF 4 ] . Siitä lähtien entsyymien korkea selektiivisyys ja aktiivisuus ionisissa nesteissä on osoitettu monissa prosesseissa. Lisäksi ioniset nesteet voivat myös vaikuttaa stabiilisuuteen, enantioselektiivisyyteen ja katalyyttiseen aktiivisuuteen. Ionisissa nesteissä aktiiviset entsyymiluokat sisältävät proteaaseja , lipaaseja, esteraaseja , glykosidaaseja ja oksidoreduktaaseja . Sekä yksivaiheista että kaksivaiheista järjestelmää voidaan käyttää muunnoksiin. Entsyymien lisäksi voidaan käyttää myös kokonaisia soluja. Käytettäessä kaksivaiheisessa järjestelmässä veden kanssa entsyymi voidaan immobilisoida ioniseen nesteeseen. Vaihtamalla ionisen nesteen liukoisuutta voidaan käyttää myös seoksia veden kanssa.
Suuret sovellukset
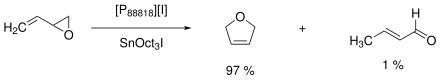
2,5-dihydrofuraani
Ensimmäinen laajamittainen sovellus, jossa käytettiin ionista nestettä, oli Eastman Chemicalin isomerointiprosessi . Prosessi kesti vuosien 1996 ja 2004 välisenä aikana ja tuotti jopa 1400 tonnia vuodessa . Se oli 2,5-dihydrofuraani päässä buteeni, 3,4-epoksi-1- valmistettiin perus Lewis katalyyttinä toimi trioktyylitina jodidia Lewis-happoa ja tetra fosfonium- perustuva ioninen neste ([P 88818 ] [I]). Jatkuvassa prosessissa katalyyttiseos voitaisiin erottaa tuotteesta ja kierrättää. Saadaan sivutuotteina krotonaldehydiä (1%) ja oligomeerejä (2%).
BASIL -prosessi
Metyyli -imidatsoliumkloridin kanssa BASF käyttää ionista nestettä BASIL -prosessissa ( kaksivaiheinen haponpoisto käyttämällä ionisia nesteitä ). Tässä tapauksessa 1-metyyli-imidatsolia käytettiin apuaineena muodostuneen suolahapon neutraloimiseksi. Prosessissa muodostuu ioninen neste, joka erottuu toiseksi faasiksi ja voidaan siten helposti erottaa. Prosessin tuottavuutta voitaisiin lisätä 80 000 kertoimella. Aiemmin tertiääristä amiinia lisättiin metyyli -imidatsolin sijasta, mutta tämä muodosti suolaa suolahapon kanssa, jota oli vaikea erottaa. Dietoksifenyylifosfiini saadaan BASIL -prosessissa.
ISOALKY -prosessi
ISOALKY -prosessilla tuotetaan alkylaattia, jota käytetään polttoaineissa korkean oktaaniluvunsa vuoksi. Ioninen neste korvaa tavalliset happamat katalyytit rikkihappo ja fluorivetyhappo . Ioniset nesteet ovat kloridisuolaa, johon lisätään alumiinitrikloridia ja pieni määrä kloorivetyä . Näin muodostuu katalyyttisesti aktiivinen superhappo . Tarkka koostumus ei ole julkinen. Kationit ovat pyridinium- ja imidatsoliumpatentoituja rakenteita. Mahdollinen katalyytti olisi esim. B. 1-butyyli-3-metyyli-imidatsoliumtetrakloorialuminaatti , joka voidaan saada 1-butyyli-3-metyyli-imidatsoliumkloridista ja alumiinitrikloridista.
Ionikompressorit
Ionikompressorit ovat iskutilavuuskompressoreita, joiden pääasiallinen käyttöalue on vedynpuristus. Ioninesteet korvaavat muuten kiinteän männän, mikä tarkoittaa, että on käytettävä vähemmän liikkuvia osia, mikä johtaa lopulta energiansäästöön. Lisäksi kompressorin rakenne yksinkertaistuu vedyn heikon liukoisuuden vuoksi käytettäviin ioninesteisiin. Linde Group on tämän alan edelläkävijä ja pystyi suunnitella ionista kompressori, joka saavutetaan paineet välillä 45 ja 90 MPa, ja jonka kapasiteetti on 8-30 kg h -1 . Erityisesti imidatsoliumpohjaisia ionisia nesteitä tutkitaan tällä sovellusalueella.
Energiset ioniset nesteet
Energisiä ionisia nesteitä (EIL) pidetään vaihtoehtoina polttoaineille ja räjähteille. Korkean energian anionit ja kationit yhdistetään. Energeettisissä ioninesteissä kationina käytetään imidatsoliumia, triatsoliumia, tetratsoliumia ja kvaternaarisia ammoniumyhdisteitä, esimerkiksi azideja, tretratsolaatteja, pikraatteja, nitraatteja tai atsolaatteja anioneina. Hypergoliset ioniset nesteet sisältävät z. B. disyaaniamidi, nitrosyanamidi, monimutkaiset alumiinianionit, hypofosfiitti- ja booripohjaiset ionit, erityisesti ne, joissa on runsaasti BH-sidoksia. Ensimmäiset hypergolisia ominaisuuksia sisältävät ioninesteet julkaistiin vuonna 2008. Tätä varten käytettiin disyaaniamidianioneja.
Ympäristön tasapaino ja toksikologia
Ionisia nesteitä kutsutaan usein "vihreiksi" vaihtoehdoiksi orgaanisille liuottimille. Tämä johtuu pääasiassa niiden korkeasta lämpöstabiilisuudesta ja alhaisesta höyrynpaineesta. Tämän seurauksena ne eivät pääse ilmakehään, jossa ne muodostavat savu-, hyökkäävät otsonikerrokseen ja edistävät ilmastonmuutosta. Myös altistuminen ihmisille ja ympäristölle ilman kautta on poissuljettu. Toinen orgaanisten liuottimien aiheuttama vaara on räjähtävien ilmaseosten muodostuminen. Tätä turvallisuusriskiä ei ole myöskään ionisten nesteiden kanssa.
Vaikka ionisten nesteiden haihtumisesta on vain vähän vaaraa, on otettava huomioon liukoisuus veteen ja siten sen saastuminen, minkä vuoksi ionisten nesteiden pitkäaikaisia ympäristövaikutuksia tutkitaan edelleen. Myös ionisten nesteiden toksikologiaa tutkitaan yhä enemmän. Erityistä huomiota kiinnitetään vesieliöihin, mutta myös mikro -organismeihin, sukkulamatoon Caenorhabditis elegans , kärkirakon etanaan ( Physella acuta ), rottiin ja seeprakalaan ( Danio rerio ). Imidatsoliumpohjaisten ionisten nesteiden valohajoavuuden puute tarkoittaa, että ne voivat kerääntyä vesistöihin, koska niiden biohajoavuus on myös erittäin alhainen. Systeemisiä tutkimuksia on tehty mm. B. suoritettu Daphnialla . Voidaan havaita, että kationin pidemmät alkyyliketjut johtavat suurempaan myrkyllisyyteen. Tämä suuntaus havaittiin imidatsolium-, pyridinium-, ammonium- ja fosfoniumioni -nesteillä. Anionien vaikutus Daphniaan ei seuraa selvää suuntausta, mutta vastaavan anionin natriumsuolaan verrattuna ioninen neste on aina myrkyllisempi. Lactobacillus -bakteeri osoittaa vähemmän aktiivisuutta maitohapon tuotannossa ionisten nesteiden [BMIM] [PF 6 ] , [HMIM] [PF 6 ] ja [OMIM] [PF 6 ] läsnä ollessa . Tässäkin on havaittavissa suuntaus, että pidemmillä alkyyliketjuilla on suurempi negatiivinen vaikutus.
Halogeeneja sisältävät ioninesteet ovat myös ympäristölle haitallisia, samoin kuin halogenoidut orgaaniset aineet, koska niitä on ympäristössä pitkään ja vain pienen määrän energiaa (valo, lämpö, entsyymit jne.) Muodostavat reaktiivisia välivaiheita, kuten radikaalit, joita löytyy sekä ilmakehästä että kehoista, ovat yhtä haitallisia. Vaikka yhdisteiden haihtuvuuden vuoksi ei ole olemassa hengitysmyrkytyksen riskiä, jätevesi voi olla ongelmallista. Mahdollisten yhdistelmien suuren määrän vuoksi halutaan kuitenkin saavuttaa halutut fysikaalis-kemialliset ominaisuudet mahdollisimman pienellä myrkyllisyydellä keskipitkällä aikavälillä.
nettilinkit
kirjallisuus
- Thomas Waldmann, Hsin-Hui Huang, Harry E.Hoster, Oliver Höfft, Frank Endres, R.Jürgen Behm: Ionic Liquid Adlayerin kuvantaminen skannaamalla tunnelimikroskopia kiinteässä | Tyhjiöliitäntä. Julkaisussa: ChemPhysChem. 12, 2011, s. 2565-2567, doi: 10.1002 / cphc.201100413 . (Ionisoidun nesteen adsorboidut yksikerroksiset kuvat kuvatulla skannaavalla tunnelimikroskoopilla)
- Nestemäinen / kiinteä käyttöliittymä erittäin ohuille ionikoneille. Julkaisussa: Langmuir . 27, 2011, s. 3662-3671, doi: 10.1021 / la105007c .
Yksilöllisiä todisteita
- ↑ Christopher P.Fredlake, Jacob M.Crosthwaite, Daniel G.Hert, Sudhir NVK Aki, Joan F.Brennecke: Imidatsoliumpohjaisten ionisten nesteiden termofysikaaliset ominaisuudet . Julkaisussa: Journal of Chemical & Engineering Data . nauha 49 , ei. 4 , heinäkuu 2004, ISSN 0021-9568 , s. 954-964 , doi : 10.1021 / je034261a .
- ^ Daniel, Claus., Besenhard, Jürgen O.: Käsikirja paristomateriaaleista . Toinen, täysin rev. ja laajennettu painos. Wiley-VCH Verlag, Weinheim 2011, ISBN 978-3-527-63720-1 .
- ↑ a b c Ana PM Tavares, Oscar Rodriguez, Eugenia A.Macedo: Entsymaattiseen biokatalyysiin sovelletut uudet ionisten nesteiden sukupolvet . Julkaisussa: Ionic Liquids - New Perspects for the Future . InTech, 2013, ISBN 978-953-510-937-2 , doi : 10.5772 / 51897 .
- ^ A b William Ramsay: XXXIV. Pikoliinista ja sen johdannaisista . Julkaisussa: The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science . nauha 2 , ei. 11. lokakuuta 1876, ISSN 1941-5982 , s. 269-281 , doi : 10.1080 / 14786447608639105 .
- ↑ a b c d Paavali. Murrill: PIKOLIINIHALIDIT JA PERHALIDIT. Julkaisussa: Journal of the American Chemical Society . nauha 21 , ei. 10. lokakuuta 1899, ISSN 0002-7863 , s. 828-854 , doi : 10.1021 / ja02060a002 .
- ↑ Gerhard Laus, Gino Bentivoglio, Herwig Schottenberger, Volker Kahlenberg, Holge Kopacka, Thomas Röder, Herbert Sixta: Ioniset nesteet: Nykyinen kehitys, mahdollisuudet ja haitat teollisissa sovelluksissa . Julkaisussa: Lenzinger reportments . nauha 84 , 2005, s. 71-85 .
- ↑ a b c d Juliusz Pernak, Tomasz Rzemieniecki, Katarzyna Materna: Ioniset nesteet "pähkinänkuoressa" (historia, ominaisuudet ja kehitys) . Julkaisussa: CHEMICS . nauha 70 , ei. 9 , 2016, s. 471-480 .
- ^ A b c d John S. Wilkes: Lyhyt historia ionisista nesteistä - sulaista suoloista neoteerisiin liuottimiin . Julkaisussa: Green Chemistry . nauha 4 , ei. 2 , 16. huhtikuuta 2002, s. 73-80 , doi : 10.1039 / b110838g .
- ↑ Friedel, C. Crafts, JM (1877) "Sur une nouvelle méthode générale de synthèse d'hydrocarbures, d'acétones jne.", Ks. Repiä. , 84 : 1392 ja 1450 .
- ^ S. Gabriel, J. Weiner: Tietoja vinyyliamiinista ja bromietyyliamiinista . Julkaisussa: Reports of the German Chemical Society . nauha 21 , ei. 2. heinäkuuta 1888, s. 2664–2669 , doi : 10.1002 / cber.18880210287 .
- ↑ Tom Welton: Ioniset nesteet: lyhyt historia . Julkaisussa: Biophysical Reviews . nauha 10 , ei. 3. kesäkuuta 2018, ISSN 1867-2450 , s. 691-706 , doi : 10.1007 / s12551-018-0419-2 , PMID 29700779 , PMC 5988633 (ilmainen koko teksti).
- ↑ a b P. Walden julkaisussa: tiedote Akad. Sei. Pietari . 1914, s. 405-422.
- ↑ Samuel Sugden, Henry Wilkins: CLXVII - Laskuvarjo ja kemiallinen rakenne. Osa XII. Sulaneet metallit ja suolat . Julkaisussa: J. Chem. Soc. nauha 0 , ei. 0 , 1929, ISSN 0368-1769 , s. 1291-1298 , doi : 10,1039 / JR9290001291 .
- ^ A b Frank H. Hurley, Thomas P. Wier: Fuusioituneiden kvaternaaristen ammoniumsuolojen metallien sähköinen levitys . Julkaisussa: Journal of The Electrochemical Society . nauha 98 , ei. 5 , 1951, s. 203 , doi : 10.1149 / 1.2778132 .
- ↑ John T.Yoke, Joseph F.Weiss, Gordon Tollin: Trietyyliamiinin reaktiot kupari (I) ja kupari (II) halogenidien kanssa . Julkaisussa: Epäorgaaninen kemia . nauha 2 , ei. 6 , joulukuu 1963, ISSN 0020-1669 , s. 1210-1216 , doi : 10.1021 / ic50010a028 .
- ↑ Nathan Kornblum, Gerald P.Coffey : Trietyylioksoniumfluoriboraatin reaktio a-pyridonin natriumsuolan kanssa 1 . Julkaisussa: The Journal of Organic Chemistry . nauha 31 , ei. 10. lokakuuta 1966, ISSN 0022-3263 , s. 3449-3451 , doi : 10.1021 / jo01348a536 .
- ↑ George W. Parshall: Katalyysi sulassa suola -aineessa . Julkaisussa: Journal of the American Chemical Society . nauha 94 , ei. 25. joulukuuta 1972, ISSN 0002-7863 , s. 8716-8719 , doi : 10.1021 / ja00780a013 .
- ↑ a b Michael Freemantle: Johdatus ionisiin nesteisiin . RSC Pub, Cambridge, UK 2010, ISBN 978-1-84755-161-0 , s. 8-10 .
- ^ RJ Gale, B.Gilbert, RA Osteryoung: Raman-spektrit sulasta alumiinikloridista: 1-butyylipyridiniumkloridijärjestelmät ympäristön lämpötiloissa . Julkaisussa: Epäorgaaninen kemia . nauha 17 , ei. 10 , 1. lokakuuta 1978, ISSN 0020-1669 , s. 2728-2729 , doi : 10.1021 / ic50188a008 .
- ↑ Patentti US4122245A : AlCl3 / 1-alkyylipyridiniumkloridin huoneenlämpöiset elektrolyytit. Julkaistu 24. lokakuuta 1978 , Keksijät: John C.Nardi, Charles L.Hussey, Lowell A.King.
- ↑ John S.Wilkes, Joseph A.Levisky, Robert A.Wilson, Charles L.Hussey : Dialkyyli-imidatsolium-kloorialuminaatin sulat: uusi huoneenlämpöisten ioninesteiden luokka sähkökemiaan, spektroskopiaan ja synteesiin . Julkaisussa: Epäorgaaninen kemia . nauha 21 , ei. 3 , maaliskuu 1982, ISSN 0020-1669 , s. 1263-1264 , doi : 10.1021 / ic00133a078 .
- ↑ Towner B. Schefflerin, Charles L. Hussey, Kenneth R. Seddon, Christopher M. Kear, Phillip D. Armitage: Molybdeeni kloori komplekseja huoneen lämpötilassa chloroaluminate ionisten nesteiden: vakauttaminen hexachloromolybdate (2-) ja hexachloromolybdate (3-) . Julkaisussa: Epäorgaaninen kemia . nauha 22 , ei. 15. heinäkuuta 1983, ISSN 0020-1669 , s. 2099-2100 , doi : 10,1021 / ic00157a001 .
- ^ Slaton E. Fry, Norbert J. Pienta: Sulatettujen suolojen vaikutukset reaktioihin. Nukleofiilinen aromaattinen substituutio halogenidi -ioneilla sulassa dodekyylitributyylifosfoniumsuolassa . Julkaisussa: Journal of the American Chemical Society . nauha 107 , ei. 22. lokakuuta 1985, ISSN 0002-7863 , s. 6399-6400 , doi : 10.1021 / ja00308a045 .
- ↑ Jeffrey A. Boon, Joseph A. Levisky, J. Lloyd Pflug, John S. Wilkes: Friedel-Crafts-reaktiot ympäristön lämpötilan sulatetuissa suoloissa . Julkaisussa: The Journal of Organic Chemistry . nauha 51 , ei. 4 , helmikuu 1986, ISSN 0022-3263 , s. 480-483 , doi : 10.1021 / jo00354a013 .
- ^ A b John S. Wilkes, Michael J. Zaworotko: Ilma- ja vedenkestävät 1-etyyli-3-metyyli-imidatsoliumpohjaiset ioninesteet . Julkaisussa: Journal of the Chemical Society, Chemical Communications . Ei. 13 , 1992, ISSN 0022-4936 , s. 965 , doi : 10.1039 / c39920000965 .
- ↑ Pierre Bonhôte, Ana-Paula Dias, Nicholas Papageorgiou, Kuppuswamy Kalyanasundaram, Michael Grätzel: Hydrofobiset, erittäin johtavat ympäristön lämpötilan sulasuolat † . Julkaisussa: Epäorgaaninen kemia . nauha 35 , ei. 5 , tammikuu 1996, ISSN 0020-1669 , s. 1168-1178 , doi : 10.1021 / ic951325x .
- ↑ a b c d e f G. Wytze Meindersma, Matthias Maase, André B. De Haan: Ionic Liquids . Julkaisussa: Ullmann's Encyclopedia of Industrial Chemistry . Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Saksa 2007, ISBN 978-3-527-30673-2 , s. 547-575 , doi : 10.1002 / 14356007.l14_l01 .
- ^ A b c d Peter Wasserscheid, Wilhelm Keim: Ioniset nesteet - uusia ratkaisuja siirtymämetallikatalyysiin . Julkaisussa: Angewandte Chemie International Edition . nauha 39 , ei. 21 , 2000, ISSN 1521-3773 , s. 3772-3789 , doi : 10.1002 / 1521-3773 (20001103) 39: 213.0.CO; 2-5 .
- ↑ a b c d e Peter Wasserscheid, T. Welton: Ioninesteet synteesissä . Wiley-VCH, Weinheim 2003, ISBN 3-527-60544-4 , s. 7-21 .
- ↑ Tietolomake 1-butyyli-3-metyyli-imidatsoliumkloridi (PDF) Carl Rothilta , saatavana 21. maaliskuuta 2021.
- ^ Joan Fuller, Richard T.Carlin, Hugh C.De Long, Dustin Haworth: 1-etyyli-3-metyyli-imidatsoliumheksafluorifosfaatin rakenne: malli huoneenlämpöisille suoloille . Julkaisussa: Journal of the Chemical Society, Chemical Communications . Ei. 3 , 1994, ISSN 0022-4936 , s. 299 , doi : 10.1039 / c39940000299 .
- ↑ a b Tamar L. Greaves, Calum J. Drummond: Protic Ionic Liquids: Properties and Applications . Julkaisussa: Chemical Reviews . nauha 108 , ei. 1. tammikuuta 2008, ISSN 0009-2665 , s. 206-237 , doi : 10.1021 / cr068040u .
- ^ A b c d Adam J. Greer, Johan Jacquemin, Christopher Hardacre: Industrial Applications of Ionic Liquids . Julkaisussa: Molecules . nauha 25 , ei. 21 , 9. marraskuuta 2020, ISSN 1420-3049 , s. 5207 , doi : 10.3390 / molekyylit25215207 , PMID 33182328 , PMC 7664896 (ilmainen koko teksti).
- ^ Paul Nancarrow, Hanin Mohammed: Ioniset nesteet avaruusteknologiassa - nykyiset ja tulevat trendit . Julkaisussa: ChemBioEng Reviews . nauha 4 , ei. 2. huhtikuuta 2017, s. 106–119 , doi : 10.1002 / cben.201600021 .
- ↑ Qinghua Zhang, Jean'ne M.Shreeve: Energiset ioniset nesteet räjähteinä ja ponneaineina: Ionisen nestekemian uusi matka . Julkaisussa: Chemical Reviews . nauha 114 , ei. 20 , 22. lokakuuta 2014, ISSN 0009-2665 , s. 10527-10574 , doi : 10.1021 / cr500364t .
- ↑ Masayoshi Watanabe, Morgan L. Thomas, Shiguo Zhang, Kazuhide Ueno, Tomohiro Yasuda: Ionisten nesteiden soveltaminen energian varastointi- ja muuntamateriaaleihin ja -laitteisiin . Julkaisussa: Chemical Reviews . nauha 117 , ei. 10 , 24. toukokuuta 2017, ISSN 0009-2665 , s. 7190-7239 , doi : 10.1021 / acs.chemrev.6b00504 .
- ↑ Yansong Zhao, Tobias Bostrom: Ionisten nesteiden käyttö aurinkokennoissa ja akuissa: katsaus . Julkaisussa: Current Organic Chemistry . nauha 19 , ei. 6. huhtikuuta 2015, s. 556-566 , doi : 10.2174 / 1385272819666150127002529 .
- ↑ a b c Peter Wasserscheid, T. Welton: Ioninesteet synteesissä . Wiley-VCH, Weinheim 2003, ISBN 3-527-60544-4 , s. 41-55 .
- ↑ b Pamela M. Dean, Jennifer M. Pringle, Douglas R. MacFarlane: rakenneanalyysi sulamispiste on alhainen orgaanisten suolojen: näkökulmia ionisten nesteiden . Julkaisussa: Physical Chemistry Chemical Physics . nauha 12 , ei. 32 , 2010, ISSN 1463-9076 , s. 9144 , doi : 10.1039 / c003519j .
- ↑ a b c Sankaran Murugesan, Oliver A. Quintero, Brendan P. Chou, Penghao Xiao, Kyusung Park: Leveä sähkökemiallinen ikkuna- ionisuola käytettäväksi elektropositiivisissa metallielektrodipositio- ja puolijohde-litiumioniakkuissa . Julkaisussa: J. Mater. Chem. . nauha 2 , ei. 7 , 2014, ISSN 2050-7488 , s. 2194-2201 , doi : 10.1039 / C3TA15010K .
- ↑ a b c Peter Wasserscheid, T. Welton: Ioninesteet synteesissä . Wiley-VCH, Weinheim 2003, ISBN 3-527-60544-4 , s. 103-126 .
- ↑ a b Fred van Rantwijk, Roger A. Sheldon: Biokatalyysi Ionic Liquidsissa . Julkaisussa: Chemical Reviews . nauha 107 , ei. 6. kesäkuuta 2007, ISSN 0009-2665 , s. 2757-2785 , doi : 10.1021 / cr050946x .
- ↑ a b Christoph Roosen, Pia Müller, Lasse Greiner: Ioninesteet biotekniikassa: sovelluksia ja näkökulmia biotransformaatioihin . Julkaisussa: Applied Microbiology and Biotechnology . nauha 81 , ei. 4 , joulukuu 2008, ISSN 0175-7598 , s. 607-614 , doi : 10.1007 / s00253-008-1730-9 , PMID 18979095 , PMC 7419490 (ilmainen koko teksti).
- ↑ Thomas Waldmann, Hsin-Hui Huang, Harry E.Hoster, Oliver Höfft, Frank Endres: Imaging an Ionic Liquid Adlayer by Scanning Tunneling Microscopy at the Solid | Vacuum Interface . Julkaisussa: ChemPhysChem . nauha 12 , ei. 14 , 4. lokakuuta 2011, s. 2565-2567 , doi : 10.1002 / cphc.201100413 .
- ↑ Martina B.Hanel, Andreas Filzwieser, Iris Filzwieser, Stefan Ruhs: ILTEC - METTOPIN VALlankumouksellinen jäähdytysratkaisu terästeollisuudelle. Haettu 9. huhtikuuta 2019 .
- ↑ a b U. Vagt: Ioniset nesteet - ainutlaatuisia materiaaleja monipuolisilla mahdollisuuksilla. Julkaisussa: CHEManager. 22/2008, s.19.
- ↑ Wu Xu, Xilin Chen, Fei Ding, Jie Xiao, Deyu Wang: Uusinta tutkimusta uusimmista vedettömistä karbonaattielektrolyytteistä 5 V: n litiumioniakkusovelluksissa . Julkaisussa: Journal of Power Sources . nauha 213 , syyskuu 2012, s. 304-316 , doi : 10.1016 / j.jpowsour.2012.04.031 .
- ↑ Michel Armand , Frank Endres , Douglas R.MacFarlane, Hiroyuki Ohno, Bruno Scrosati: Ionic-nestemäiset materiaalit tulevaisuuden sähkökemiallisiin haasteisiin . Julkaisussa: Nature Materials . nauha 8 , ei. 8. elokuuta 2009, ISSN 1476-1122 , s. 621-629 , doi : 10.1038 / nmat2448 .
- ↑ A. Guerfi, M. Dontigny, P. Charest, M. Petitclerc, M. Lagacé: Parannettu elektrolyyttejä, Li-ioni-akkuja: seokset ionisen nesteen ja orgaaninen elektrolyytti, jossa on parannettu turvallisuus ja sähkökemiallista suorituskykyä . Julkaisussa: Journal of Power Sources . nauha 195 , ei. 3 , helmikuu 2010, s. 845-852 , doi : 10.1016 / j.jpowsour.2009.08.056 .
- ↑ Richard P.Swatloski, Scott K.Spear, John D.Holbrey, Robin D.Rogers: Selluloosan liukeneminen ionisten nesteiden kanssa . Julkaisussa: Journal of the American Chemical Society . nauha 124/18 , 2002, s. 4974–4975 , doi : 10.1021 / ja025790m .
- ↑ Hao Zhang, Jin Wu, Jun Zhang, Jiasong Hän: 1-allyyli-3-metyyli-imidatsoliumkloridi Huoneenlämpötila-ioninen neste: Uusi ja tehokas ei-johdannainen selluloosalle . Julkaisussa: Makromolekyylit . nauha 38 , 2005, s. 8272-8277 , doi : 10.1021 / ma0505676 .
- ↑ Bin Zhao, Lasse Greiner, Walter Leitner: Selluloosan liukoisuus karboksylaattipohjaisiin ioninesteisiin . Julkaisussa: RSC Advances . nauha 2 , 2012, s. 2476-2479 , doi : 10.1039 / C2RA01224C .
- ↑ Frank Hermanutz, Frank Gähr, Klemens Massonne, Eric Uerdingen: Suullinen esitys 45. tekokuitukonferenssissa . Dornbirn, Itävalta, 20. - 22. syyskuuta 2006.
- ^ Y. Su, HM Brown, X. Huang, X. Zhou, JE Amonette, ZC Zhang: Selluloosan yksivaiheinen muuntaminen 5-hydroksimetyylifurfuraaliksi (HMF), joka on monipuolinen alustamikaali . Julkaisussa: Appl. Katalyysi . A 361, 2009, s. 117-122. doi: 10.1016 / j.apcata.2009.04.002
- ^ Foorumi: Chem. Ing. Tech. 6/2009 . Julkaisussa: Chemical Engineer Technology . nauha 81 , ei. 6 , 2009, ISSN 1522-2640 , s. 679 , doi : 10.1002 / cite.200990045 .
- ↑ a b c I.M. Marrucho, LC Branco, LPN Rebelo: Ioniset nesteet farmaseuttisissa sovelluksissa . Julkaisussa: Annual Review of Chemical and Biomolecular Engineering . nauha 5 , ei. 1 , 7. kesäkuuta 2014, ISSN 1947-5438 , s. 527-546 , doi : 10.1146 / annurev-chembioeng-060713-040024 .
- ↑ Jelena Stoimenovski, Douglas R.MacFarlane, Katharina Bica, Robin D.Rogers: Aktiivisten farmaseuttisten ainesosien kiteinen ja ioninen nestesuolamuoto : Position Paper . Julkaisussa: Pharmaceutical Research . nauha 27 , ei. 4. huhtikuuta 2010, ISSN 0724-8741 , s. 521-526 , doi : 10.1007 / s11095-009-0030-0 .
- ^ A b Sónia N.Pedro, Carmen SR Freire, Armando JD Silvestre, Mara G.Freire: Ionisten nesteiden rooli farmaseuttisella alalla: yleiskatsaus asiaan liittyvistä sovelluksista . Julkaisussa: International Journal of Molecular Sciences . nauha 21 , ei. 21. marraskuuta 2020, ISSN 1422-0067 , s. 8298 , doi : 10.3390 / ijms21218298 , PMID 33167474 , PMC 7663996 (ilmainen koko teksti).
- ^ Whitney L.Hough, Marcin Smiglak, Héctor Rodríguez, Richard P.Swatloski, Scott K.Spear: Ionisten nesteiden kolmas kehitys: aktiiviset farmaseuttiset ainesosat . Julkaisussa: New Journal of Chemistry . nauha 31 , ei. 8. heinäkuuta 2007, ISSN 1369-9261 , s. 1429-1436 , doi : 10.1039 / B706677P .
- ↑ J. Stoimenovski, DR MacFarlane, K. Bica, RD Rogers: Crystalline vs. Ionic Liquid Salt Forms of Active Pharmaceutical Components: A Position Paper . Julkaisussa: Pharmaceutical Research . nauha 27 , 2010, s. 521-526 , doi : 10.1007 / s11095-009-0030-0 .
- ↑ a b c d Caroline Emilie Paul, Vicente Gotor Fernández: Biokatalyysi ja biotransformaatio ioniliuoksissa . Julkaisussa: Ionic Liquids in Lipid Processing and Analysis . Elsevier, 2016, ISBN 978-1-63067-047-4 , s. 11-58 , doi : 10.1016 / b978-1-63067-047-4.00002-7 .
- ^ R. Madeiran Lau, F. Van Rantwijk, KR Seddon, RA Sheldon: Lipaasin katalysoima reaktiot ioninesteitä . Julkaisussa: Organic Letters . nauha 2 , ei. 26. joulukuuta 2000, ISSN 1523-7060 , s. 4189-4191 , doi : 10.1021 / ol006732d .
- ↑ Eduardo García-Verdugo, Belen Altava, M. Isabel Burguete, Pedro Lozano, SV Luis: Ioniset nesteet ja jatkuvan virtauksen prosessit: hyvä avioliitto kestävien prosessien suunnitteluun . Julkaisussa: Green Chemistry . nauha 17 , ei. 5 , 2015, ISSN 1463-9262 , s. 2693-2713 , doi : 10.1039 / C4GC02388A .
- ↑ Tom Welton: Liuottimet ja kestävä kemia . Julkaisussa: Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences . nauha 471 , ei. 2183 , 8. marraskuuta 2015, ISSN 1364-5021 , s. 20150502 , doi : 10.1098 / rspa.2015.0502 , PMID 26730217 , PMC 4685879 (ilmainen koko teksti) - (englanti).
- ↑ Patentti US7432409B2 : Alkylointiprosessi käyttäen kloorialuminaatti -ionisia nestemäisiä katalyyttejä. Julkaistu 21. joulukuuta 2004 , Keksijät: S. Elomari, S. Trumbull, HKC Timken, R. Cleverdon.
- ↑ Hye Kyung Timken, Huping Luo, Bong-Kyu Chang, Elizabeth Carter, Matthew Cole: ISOALKY ™ -teknologia: seuraavan sukupolven alkylaatit bensiinin valmistusprosessiteknologia, jossa käytetään nestemäistä ionikatalyyttiä . Julkaisussa: Ionic Liquids Commercial Applications . Springer International Publishing, Cham 2020, ISBN 978-3-03035244-8 , s. 33-47 , doi : 10.1007 / 978-3-030-35245-5_2 .
- ↑ a b Jiexin Zou, Ning Han, Jiangyan Yan, Qi Feng, Yajun Wang: Sähkökemialliset pakkaustekniikat korkeapaineiselle vedylle: nykytila, haasteet ja näkökulma . Julkaisussa: Electrochemical Energy Reviews . nauha 3 , ei. 4. joulukuuta 2020, ISSN 2520-8489 , s. 690-729 , doi : 10.1007 / s41918-020-00077-0 .
- ↑ Marzena Dzida, Małgorzata Musiał, Edward Zorębski, Sylwia Jężak, Justyna Skowronek: Vertaileva tutkimus on High Pressure Termofysikaaliset ominaisuudet 1-etyyli-3-metyyli-ja 1,3-Diethylimidazolium etyyli Sulfaatit käytettäväksi kestävän ja tehokas Hydraulinesteet . Julkaisussa: ACS Sustainable Chemistry & Engineering . nauha 6 , ei. 8. elokuuta 2018, ISSN 2168-0485 , s. 10934-10943 , doi : 10.1021 / acssuschemeng.8b02318 .
- ↑ Nasrin Arjomand Kermani, Irina Petrushina, Aleksey Nikiforov, Jens Oluf Jensen, Masoud Rokni: Ionisen nestemäisen vetykompressorin rakennusmateriaalien korroosiokäyttäytyminen . Julkaisussa: International Journal of Hydrogen Energy . nauha 41 , ei. 38 , lokakuu 2016, s. 16688-16695 , doi : 10.1016 / j.ijhydene.2016.06.221 .
- ↑ Qiu-Han Lin, Yu-Chuan Li, Ya-Yu Li, Zhu Wang, Wei Liu: Energiset suolat, jotka perustuvat 1-amino-1,2,3-triatsoliin ja 3-metyyli-1-amino-1,2, 3-triatsolit . Julkaisussa: Journal of Materials Chemistry . nauha 22 , ei. 2 , 8. joulukuuta 2011, ISSN 1364-5501 , s. 666-674 , doi : 10.1039 / C1JM14322K .
- ↑ Qinghua Zhang, Jean'ne M.Shreeve: Energiset ioniset nesteet räjähteinä ja ponneaineina: Ionisen nestekemian uusi matka . Julkaisussa: Chemical Reviews . nauha 114 , ei. 20 , 22. lokakuuta 2014, ISSN 0009-2665 , s. 10527-10574 , doi : 10.1021 / cr500364t .
- ^ Stefan Schneider, Tom Hawkins, Yonis Ahmed, Stephan Deplazes, Jeff Mills: Ionic Liquid Fuels for Chemical Propulsion . Julkaisussa: ACS Symposium Series . nauha 1117 . American Chemical Society, Washington, DC 2012, ISBN 978-0-8412-2763-7 , s. 1–25 , doi : 10.1021 / bk-2012-1117.ch001 .
- ↑ Stefan Schneider, Tommy Hawkins, Michael Rosander, Ghanshyam Vaghjiani, Steven Chambreau: Ionic Liquids as Hypergolic Fuels . Julkaisussa: Energy & Fuels . nauha 22 , ei. 4 , 1. heinäkuuta 2008, ISSN 0887-0624 , s. 2871-2872 , doi : 10.1021 / ef800286b .
- ↑ a b c Jolanta Flieger, Michał Flieger: Ionisten nesteiden myrkyllisyys - hyödyt ja uhat . Julkaisussa: International Journal of Molecular Sciences . nauha 21 , ei. 17. , 29. elokuuta 2020, ISSN 1422-0067 , s. 6267 , doi : 10.3390 / ijms21176267 , PMID 32872533 , PMC 7504185 (ilmainen koko teksti).
- ↑ a b c d Dongbin Zhao, Yongcheng Liao, Ziding Zhang: Ionic Liquids -toksisuus . Julkaisussa: CLEAN - maaperä, ilma, vesi . nauha 35 , ei. 1 , helmikuu 2007, s. 42-48 , doi : 10.1002 / clen.200600015 .
- ↑ N. Gathergood, PJ Scammells: Biohajoavia sivuketjuja sisältävien huoneenlämpöisten ioninesteiden suunnittelu ja valmistus . Julkaisussa: Australian Journal of Chemistry . nauha 55 , ei. 9 , 2002, ISSN 0004-9425 , s. 557 , doi : 10.1071 / CH02148 .
- ↑ Andrew S. Wells, Vyvyan T.Combe: Joidenkin tavallisten ioninesteiden makean veden ekotoksisuudesta ja biohajoavuusominaisuuksista . Julkaisussa: Organic Process Research & Development . nauha 10 , ei. 4 , heinäkuu 2006, ISSN 1083-6160 , s. 794-798 , doi : 10.1021 / op060048i .
- ^ Mineraali-orgaanisten ja mikro-organismien vuorovaikutusten vaikutus maaperän ja makean veden ympäristöihin . Springer US, Boston, MA 1999, ISBN 978-1-4613-7120-5 , doi : 10.1007 / 978-1-4615-4683-2 .
- ↑ Michiaki Matsumoto, Kenji Mochiduki, Kei Fukunishi, Kazuo Kondo: Orgaanisten happojen uuttaminen käyttämällä imidatsoliumpohjaisia ioninesteitä ja niiden myrkyllisyys Lactobacillus rhamnosus -lajille . Julkaisussa: Erotus- ja puhdistustekniikka . nauha 40 , ei. 1 , marraskuu 2004, s. 97-101 , doi : 10.1016 / j.seppur.2004.01.009 .
- ↑ Jan C. Kuschnerow: Ionisten nesteiden käyttö katalyyttinä homogeenisessa reaktiivisessa tislauksessa ottaen huomioon reaktion kineettiset näkökohdat . GRIN Verlag, 2011, ISBN 978-3-640-94255-8 , s. 14 ( rajoitettu esikatselu Google -teoshaussa).
- ↑ Thi Phuong Thuy Pham, Chul-Woong Cho, Yeoung-Sang Yun: Ympäristön kohtalo ja ionisten nesteiden myrkyllisyys: Katsaus. Julkaisussa: Water Research. 44, 2010, s. 352, doi: 10.1016 / j.watres.2009.09.030 .
- ^ Sónia PM Ventura, Carolina S.Marques, Andreia A.Rosatella, Carlos AM Afonso, Fernando Gonçalves: Eri ionisten nesteperheiden toksisuuden arviointi Vibrio fischeri -bakteereille . Julkaisussa: Ecotoxicology and Environmental Safety . nauha 76 , helmikuu 2012, s. 162-168 , doi : 10.1016 / j.ecoenv.2011.10.006 .