Kuparioksidi
| Kristallirakenne | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
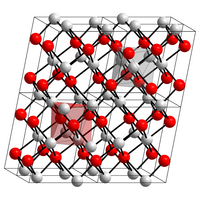
| ||||||||||||||||||||||
| __ Cu 2+ __ O 2− | ||||||||||||||||||||||
| Kristallijärjestelmä |
monokliininen |
|||||||||||||||||||||
| Avaruusryhmä |
C 2 / c (nro 15) |
|||||||||||||||||||||
| Kenraali | ||||||||||||||||||||||
| Sukunimi | Kuparioksidi | |||||||||||||||||||||
| muut nimet |
|
|||||||||||||||||||||
| Suhdekaava | CuO | |||||||||||||||||||||
| Lyhyt kuvaus |
musta, amorfinen tai kiteinen kiinteä aine |
|||||||||||||||||||||
| Ulkoiset tunnisteet / tietokannat | ||||||||||||||||||||||
| ||||||||||||||||||||||
| ominaisuudet | ||||||||||||||||||||||
| Moolimassa | 79,545 g mol -1 | |||||||||||||||||||||
| Fyysinen tila |
kiinteä |
|||||||||||||||||||||
| tiheys |
6,48 g cm -3 |
|||||||||||||||||||||
| Sulamispiste |
1326 ° C |
|||||||||||||||||||||
| kiehumispiste |
terminen hajoaminen: 1026 ° C |
|||||||||||||||||||||
| liukoisuus |
melkein liukenematon veteen, liukenee laimennettuihin happoihin, liukenee ammoniumhydroksidiin |
|||||||||||||||||||||
| turvallisuusohjeet | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
0,1 mg m −3 (mitattuna hengitettävänä aerosolijakeena) |
|||||||||||||||||||||
| Mahdollisuuksien mukaan ja tapana käytetään SI-yksiköitä . Ellei toisin mainita, annetut tiedot koskevat vakio-olosuhteita . | ||||||||||||||||||||||
Kupari (II) oksidi (aiemmin tunnettu nimellä kuparituhka , kupariruoste , palanut kupari ja kuparivasara tai kuparipuhallus sekä kuparikalkki ja latinalainen aes ustum ) on kemiallinen yhdiste, joka sisältää kuparia ja happea . Tässä oksidissa, jolla on empiirinen kaava CuO, kupari on kaksiarvoinen . Kupari (II) oksidi on musta, amorfinen tai kiteinen kiinteä aine.
Tapahtua
Kupari (II) oksidia esiintyy luonnossa kuin mineraali tenorite . Tenorite muodostetaan sään kuparin sulfidien ja on siksi yleensä löytyy hapettunut osissa kupariseoksia. Mineraali on nimetty italialaisen kasvitieteilijän Michele Tenoren mukaan .
Uuttaminen ja esittely
Kupari (II) oksidi voidaan tuottaa kupar (II) nitraatin tai emäksisen kuparikarbonaatin lämpöhajotuksella ( pyrolyysi ) .
Kupari (II) oksidia voidaan tuottaa myös kuumentamalla (juuri saostettua) kupari (II) hydroksidia . Kupari (II) -hydroksidi saostetaan lisäämällä alkalimetallihydroksideja Cu (II) -suolaliuokseen.
Kupari (II) oksidi muodostuu yhdessä kupari (I) oksidin kanssa, kun metallikupari kuumennetaan ilmassa punaiseksi.
Aikaisemmin Aes ustum saatiin asettamalla kuparilevyt kerroksittain pöytäsuolan kanssa suljettavaan upokkaaseen ja hehkuttamalla 12 tunnin ajan. Syttymisen jäännös jauhettiin ja liuotettiin vedellä.
ominaisuudet
Kupari (II) oksidi on liukenematon veteen ja alkoholeihin . Sitä vastoin se liukenee laimennettuihin happoihin . Vastaavat kupari (II) suolat voidaan saada haihduttamalla. Kupari (II) oksidi liukenee ammoniakkiveteen muodostaen komplekseja.
Kupari (II) oksidi adsorboi helposti happea, typpeä , hiilidioksidia ja muita kaasuja .
Kuumennettaessa noin 800 ° C: n yläpuolelle kupari (II) oksidi pelkistyy kupari (I) oksidiksi vapauttaen happea.
Jos metallinen kupari ja kupari (II) oksidi kuumennetaan yhdessä , muodostuu myös kupari (I) oksidi.
Korotetuissa lämpötiloissa kupari (II) oksidi pelkistetään metallikupariksi erilaisilla pelkistimillä (esim. Hiili , hiilimonoksidi , vety ).
Kun kupari (II) oksidi kuumennetaan fluorivedyllä 400 ° C: seen, muodostuu kupari (II) fluoridia .
Se on monokliininen kiderakenne, jossa tila ryhmä C 2 / C (space ryhmä ei. 15) (a = 4,683 A , b = 3,423 A, c = 5,129 Ä, β = 95,54 °). Sen muodostumisentalpia on −155,8 kJ / mol.
käyttää
Kupari (II) oksidia käytetään pigmenttinä värjäämiseen lasi , keramiikka , posliini ja keinotekoinen jalokiviä . Lisäksi se käytetään katodimateriaalina on akkuja , kuten katalysaattorina , ja rikinpoistoon ja raakaöljyn ja antifouling-maalit. Kupari (II) oksidia käytetään myös raaka-aineena erilaisten kupariyhdisteiden tuotannossa. Koska löydettiin La 2 CuO 4 -yhdisteiden (supistettu strontiumilla) suprajohtavuus ja sen jälkeen löydettiin yli sata samanlaista yhdistettä, joista suurin osa ei voi tehdä ilman kuparia ja happea, kupari (II) oksidia käytetään myös käytetyt keraamiset suprajohteet, joita pidetään tulevaisuuteen suuntautuvina materiaaleina.
Yksittäiset todisteet
- ↑ b c d e f g Merkintä kupari (II) oksidi on GESTIS aine tietokanta IFA , pääsee 7. joulukuuta, 2019. (JavaScript vaaditaan)
- ↑ Kuparioksidien merkintä . Julkaisussa: Römpp Online . Georg Thieme Verlag, luettu 13. kesäkuuta 2014.
- ↑ Merkintä kupari (II) oksidi on luokitusten ja merkintöjen luetteloon on Euroopan kemikaaliviraston (ECHA), pääsee 17. kesäkuuta 2017. Valmistajien ja jälleenmyyjien voi laajentaa yhdenmukaistettuun luokitukseen ja merkintöihin .
- ↑ Emil Ernst Ploß: Kirja vanhoista väreistä. Tekstiilivärien tekniikka keskiajalla ja näkymä kiinteisiin väreihin. 6. painos München 1989, ISBN 978-3-89164-060-9 .
- ^ Wolfgang Schneider: Farmaseuttiset kemikaalit ja mineraalit. Lisäaineet (Lääkehistorian sanaston III osaan). Frankfurt am Main 1975, s.85.
- ↑ Otto Zekert (Toim.): Dispensatorium pro pharmacopoeis Viennensibus Itävallassa 1570. Toimittanut Itävallan apteekkihenkilöstöyhdistys ja farmasian historian seura. Deutscher Apotheker-Verlag Hans Hösel, Berliini 1938, s. 133 ( Aes ).
- ↑ Mindat: tenoriitti (eng.)
- ↑ Otto Zekert (Toim.): Dispensatorium pro pharmacopoeis Viennensibus Itävallassa 1570. Toimittanut Itävallan apteekkihenkilöstöyhdistys ja farmasian historian seura. Deutscher Apotheker-Verlag Hans Hösel, Berliini 1938, s.133.
- ↑ Georg Brauer (Toim.), Yhteistyössä Marianne Baudler ja muut: Handbook of Preparative Inorganic Chemistry. 3. päivitetty painos. Osa II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 , s.979 .












