Fermium
| ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Yleisesti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nimi , symboli , atominumero | Fermium, Fm, 100 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementtiluokka | Aktinidit | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ryhmä , jakso , lohko | Ac , 7 , f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-numero | 7440-72-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomimassa | 257,0951 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomisäde (laskettu) | - (vastaa 198) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronikonfiguraatio | [ Rn ] 5 f 12 7 s 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisointienergia | 6..50 (7) eV ≈ 627 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisointienergia | 12.4 (4) eV ≈ 1 200 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisointienergia | 23.2 (4) eV ≈ 2 240 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisointienergia | 39.3 (4) eV ≈ 3 790 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisointienergia | 55.0 (1,9) eV ≈ 5 310 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysisesti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysinen tila | tiukasti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sulamispiste | (laskettu) 1125 K (noin 852 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiallisesti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hapetustilat | +2, +3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normaali potentiaali | −1,96 V (Fm 3+ + 3 e - → Fm) −2,37 V (Fm 2+ + 2 e - → Fm) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotoopit | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Katso muut isotoopit isotooppiluettelosta | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vaara- ja turvallisuustiedot | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Radioaktiivinen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Mahdollisuuksien mukaan ja tapana käytetään SI-yksiköitä . Ellei toisin mainita, annetut tiedot koskevat vakio-olosuhteita . | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Fermium on yksinomaan keinotekoisesti tuotettu kemiallinen alkuaine, jolla on elementtisymboli Fm ja atominumero 100. Jaksollisessa taulukossa se on aktinidien ryhmässä ( 7. jakso , f-lohko ) ja on myös yksi transuraanisista alkuaineista . Fermium on radioaktiivinen metalli, jota ei kuitenkaan ole vielä edustettu metallina käytettävissä olevien pienten määrien vuoksi. Se löydettiin vuonna 1952 ensimmäisen amerikkalaisen vetypommin testaamisen jälkeen ja nimettiin Enrico Fermin kunniaksi, jolla ei kuitenkaan ollut mitään tekemistä fermiumin löytämisen tai tutkimuksen kanssa.
historia


Fermium löydettiin yhdessä Einsteiniumin kanssa ensimmäisen amerikkalaisen vetypommin, Ivy Mike , testin jälkeen 1. marraskuuta 1952 Eniwetokin atollilla . Ensimmäiset näytteet saatiin suodatinpapereilta, joita kuljetettiin mukana räjähdyspilven läpi lennettäessä. Suuremmat määrät myöhemmin eristettiin koralleista. Sotilasalaisuuden vuoksi tuloksia ei alun perin julkaistu.
Alustava tutkimus räjähdyksen jäännöksistä oli osoittanut uuden plutonium-isotoopin 244 Pu muodostumisen, mikä olisi voinut johtua vain uraani- 238-ytimen ottamasta kuudesta neutronista ja kahdesta seuraavasta β-hajoamisesta .
Tuolloin uskottiin, että raskas ydin neutronien imeytyminen oli harvinaista. 244 Pu: n tunnistaminen ehdotti kuitenkin, että uraanin ytimet voivat siepata monia neutroneja, mikä johtaa uusiin alkuaineisiin.
Muodostuminen saavutettiin jatkuvalla neutronien sieppauksella : räjähdyshetkellä neutronivuon tiheys oli niin suuri, että suurin osa tällä välin muodostuneista - radioaktiivisista - atomituumista ei ollut vielä hajonnut seuraavalla neutronin sieppauksella. Hyvin korkealla neutronivirralla massaluku kasvaa jyrkästi muuttumatta atomilukua. Vasta sitten saadut epävakaat nuklidit hajoavat monien β-hajoamisten aikana stabiileiksi tai epästabiileiksi nukleideiksi, joilla on suuri atomiluku:
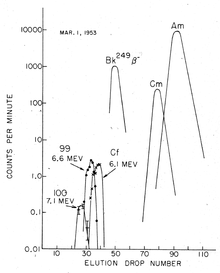
Fermiumin löytäminen ( Z = 100) vaati enemmän materiaalia, koska uskottiin, että saanto olisi ainakin suuruusluokkaa pienempi kuin elementin 99. Siksi saastuneet korallit Eniwetok-atollilta (missä testi oli tapahtunut) vietiin Kalifornian yliopiston säteilylaboratorioon Berkeleyssä Kaliforniassa käsittelyä ja analysointia varten. Liuenneet aktinidi-ionit erotettiin sitruunahappo / ammoniumsitraattipuskurin läsnä ollessa heikosti happamassa väliaineessa ( pH ≈ 3,5) ioninvaihtimien kanssa korotetussa lämpötilassa. Noin kaksi kuukautta myöhemmin eristettiin uusi komponentti, korkeaenerginen a-emitteri (7,1 MeV), jonka puoliintumisaika oli noin yksi päivä. Tällaisella lyhyellä puoliintumisaikalla se voi syntyä vain Einsteinium-isotoopin β-hajoamisesta, joten elementin 100 isotoopin oli oltava uusi: se tunnistettiin nopeasti 255 Fm: ksi (t ½ = 20,07 tuntia). .
Syyskuussa 1953 ei ollut selvää, milloin Berkeleyn , Argonnen ja Los Alamosin joukkueiden tulokset julkaistiin. Uudet elementit päätettiin tuottaa pommituskokeilla; Samalla varmistettiin, että nämä tulokset eivät kuulu salassapitovelvollisuuden piiriin ja että ne voidaan siksi julkaista. Einsteinium-isotooppeja tuotettiin pian sen jälkeen Kalifornian yliopiston säteilylaboratoriossa pommittamalla uraania ( 238 U) typellä ( 14 N). Todettiin, että tätä elementtiä on toistaiseksi pidetty salassa. Kahden äskettäin löydetyn elementin isotoopit muodostettiin säteilyttämällä plutonium-isotooppi 239 Pu, ja tulokset julkaistiin viidessä julkaisussa nopeasti peräkkäin. Lopulliset reaktiot Californiumista ovat:
Berkeleyn tiimi oli myös huolissaan siitä, että toinen tutkijaryhmä saattaisi löytää ja julkaista elementin 100 kevyempiä isotooppeja ionipommituksella ennen kuin he voisivat julkaista luokiteltuja tutkimuksia. Koska vuoden 1953 lopussa ja vuoden 1954 alussa Tukholman Nobelin fysiikan instituutin työryhmä ampui uraanin ytimiä hapen ytimillä; muodostui isotooppi, jonka massan numero 250 oli elementti 100 ( 250 μm). Yksiselitteinen tunnistus voidaan saada hajoamisen aikana emittoituneen a-hiukkasen ominaisenergian perusteella .
Berkeley-tiimi on jo julkaissut tuloksia molempien alkuaineiden kemiallisista ominaisuuksista. Lopuksi lämpöydinräjähdyksen tulokset julkaistiin vuonna 1955 ja julkaistiin sitten.
Viime kädessä Berkeley-ryhmän prioriteetti tunnustettiin yleisesti, koska heidän viisi julkaisua edeltivät ruotsalaista julkaisua, ja he voivat luottaa vuoden 1952 lämpöydinräjähdyksen aiemmin salaisiin tuloksiin. Tähän liittyi etuoikeus nimetä uudet elementit. He päättivät nimetä ne tunnettujen, kuolleiden tutkijoiden mukaan. Nimet annettiin nopeasti antaa Albert Einsteinin ja Enrico Fermin kunniaksi , jotka molemmat olivat kuolleet äskettäin: "Ehdotamme alkuaineelle, jonka atominumero on 99, einsteiniumia (symboli E) Albert Einsteinin jälkeen ja nimelle. elementille atomi numero 100, fermium (symboli Fm), kun Enrico Fermi. ”ilmoitus kahden äskettäin löydetty elementtiä Einsteinium ja fermium oli tehnyt Albert Ghiorso klo 1st Geneven Atomic konferenssissa , joka pidettiin 8.-pidettiin 20. elokuuta 1955.
Elementille annettiin myöhemmin systemaattinen nimi Unnilnilium jonkin aikaa.
Isotoopit
Kaikki tähän mennessä tiedossa olevat 19 nuklidia ja 3 ydin-isomeeriä ovat radioaktiivisia ja epävakaita. Tunnetut massanumerot vaihtelevat välillä 242 - 260. Isotoopilla 257 Fm on ylivoimaisesti pisin puoliintumisaika 100,5 päivällä, joten maapallolla ei voi olla enää luonnollisia tapahtumia. 253 Fm: n puoliintumisaika on 3 päivää, 251 Fm 5,3 tuntia, 252 Fm 25,4 tuntia, 254 Fm 3,2 tuntia, 255 Fm 20,1 tuntia ja 256 Fm 2,6 tuntia. Kaikkien muiden puoliintumisajat ovat 30 minuutista alle millisekuntiin.
Jos otetaan pois pisimpään eläneen isotoopin 257 Fm hajoaminen , niin ensin 253 Cf syntyy α-hajoamisen kautta , joka puolestaan muuttuu 253 Es : ksi β-hajoamisen kautta . Seuraava hajoaminen johtaa sitten 249 Bk: n, 249 Cf: n, 245 Cm: n, 243 Am: n, 241 Pu: n, 241 Am: n ja 237 Np: n kautta, mikä on neptunium-sarjan alku (4 n + 1).
- Annetut ajat ovat puoliintumisaikoja.
 Hajoaminen Fermium-257: stä Neptunium-sarjaan .
Hajoaminen Fermium-257: stä Neptunium-sarjaan .
Fermium-este
Fermium este on se, että fermium isotoopit 258 Fm, 259 Fm ja 260 Fm joskus hajoavat itsestään sen jälkeen, kun osa toisen (t ½ = 370 us , 1,5 s tai 4 ms). 257 Fm on α-emitteri ja hajoaa arvoon 253 Vrt. Lisäksi missään aiemmin tunnetuista fermium-isotoopeista ei ole β-hajoamisia, mikä estää mendeleviumin muodostumisen hajoamalla fermiumista. Nämä tosiasiat estävät käytännössä kaikenlaiset pyrkimykset tuottaa elementtejä, joiden atomiluku on yli 100 tai massa on suurempi kuin 257, neutronisäteilyn avulla, esimerkiksi ydinreaktorin avulla. Fermium on siis viimeinen alkuaine, joka voidaan tuottaa neutronien sieppauksella. Kaikki yritykset lisätä neutroneja fermium-ytimeen johtavat spontaaniin fissioon.
Uuttaminen
Fermiumia tuotetaan pommittamalla kevyempiä aktinideja neutroneilla ydinreaktorissa. Päälähde on 85 MW: n korkea-isotooppireaktori Oak Ridgen kansallisessa laboratoriossa Tennessee, USA: ssa, joka on perustettu transkuriumin alkuaineiden tuotantoon (Z> 96).
Oak Ridge suurempia määriä on Curium on säteilytetty ja decigram määriä Californium , milligrammamääriä berkelium ja einsteinium ja pikogrammaa suurten määrien tuottamiseksi fermium. Fermiumin nanogrammaa ja mikrogrammaa voidaan valmistaa tiettyjä kokeita varten. Lämpöydinräjähdyksissä 20 - 200 kilotonnin tuotetun fermiumin määrän uskotaan olevan muutaman milligramman luokkaa, vaikka se sekoittuu valtavaan määrään räjähdysjätteitä; 40 kilogrammaa 257 Fm: ää eristettiin 10 kilogrammasta 16. heinäkuuta 1969 tehdyn Hutch-testin räjähdyksen jäännöksistä .
Säteilytyksen jälkeen fermium on erotettava muista aktinideista ja lantanoidifissiotuotteista. Tämä saavutetaan tavallisesti ioninvaihtokromatografialla , standardimenettely suoritetaan kationinvaihtimilla, kuten Dowex 50 tai T EVA , eluoiden ammonium-a-hydroksi-isovoihappometyyliesterin liuoksella . Pienemmät kationit muodostavat vakaampia komplekseja metyyli-a-hydroksi-isobutyraatti-anionien kanssa, joten ne eluoituvat ensisijaisesti pylväästä. Nopea jakokiteytysmenetelmä on myös kuvattu.
Vaikka fermiumin vakain isotooppi on 257 Fm ja puoliintumisaika 100,5 päivää, useimmat tutkimukset perustuvat 255 Fm: iin (t ½ = 20,07 tuntia). Tämä isotooppi voidaan helposti eristää; se on 255 Es: n hajoamistuote ( t½ = 39,8 päivää).
Pienet määrät einsteiniumia ja fermiumia eristettiin ja erotettiin neutronilla säteilytetystä plutoniumista . Neljä Einsteinium isotooppien havaittiin (yksityiskohdat on puoli-elämään mitattiin aika): 253 Es (α-emitterit t ½ = 20,03 päivä, ja spontaani fissio puoli-elämän 7 x 10 5 vuotta); 254 m Es (β-säteilijät, joiden t ½ = 38,5 tuntia), 254 Es (α-säteilijät, joiden t ½ = ∼ 320 päivää) ja 255 Es (β-säteilijöiden, joiden t ½ = 24 päivää). Kaksi fermium-isotooppia löydettiin: 254 Fm (a-emitterit, joiden t 1/2 = 3,24 tuntia ja spontaanin fissio-puoliintumisaika 246 päivää) ja 255 Fm (a-emitterit, joiden t 1/2 = 21,5 tuntia).
Uraanin pommittaminen viisinkertaisella ionisoidulla typellä ja kuusinkertaisella ionisoidulla happiatomilla tuotti myös Einsteinium- ja Fermium-isotooppeja.
ominaisuudet
Kun jaksollisen , fermium kanssa atomi numero 100 on rivi aktinidien, sen edeltäjä on Einsteinium, seuraava elementti on Mendelevium . Sen analoginen että lantanidi sarjassa on erbium .
Fyysiset ominaisuudet
Metalli ei ole vielä esitetty, mutta mittaukset on tehty seokset kanssa lantanoideja , ja joitakin laskelmia tai ennusteet ovat käytettävissä. Entalpia sublimaatio on suoraan verrannollinen valenssielektroni rakenne metallia. Sublimaatio entalpia fermium määritettiin suoraan mittaamalla osapaine fermium yli FM- Sm ja Fm / Ennustettavuuden Yb seokset lämpötila-alueella 642-905 K. He saavuttivat arvon 142 (13) kJ mol −1 . Koska fermiumin sublimaatioentalpia on samanlainen kuin kaksiarvoisen einsteiniumin, europiumin ja ytterbiumin, pääteltiin, että fermiumilla on kaksiarvoinen metallinen tila. Verrattaessa europiumin, ytterbiumin ja einsteiniummetallien säteisiin ja sulamispisteisiin, fermiumille saatiin arviolta arvot 198 pm ja 1125 K.
Normaali potentiaali on arvioitu olevan samanlainen kuin ytterbium Yb 3+ / Yb 2+ pari, eli noin -1,15 V verrattuna standardi vety elektrodi , on arvo, joka yhtyy teoreettisten laskelmien. Perusteella polarografista mittausten, normaali potentiaali -2,37 V määritettiin varten Fm 2 + / Fm 0 pari. Fm 3+ voidaan pienentää Fm 2+: ksi suhteellisen helposti , esim. B. saostuu samarium (II) kloridilla yhdessä fermiumin kanssa.
Kemialliset ominaisuudet
Tähän asti fermiumin kemiaa voitiin tutkia vain liuoksessa merkkiainetekniikoiden avulla; kiinteitä yhteyksiä ei pystytty luomaan. Normaaleissa olosuhteissa, fermium on liuoksessa Fm 3+ ioni, joka on hydraatio määrä on 16,9 ja happo vakio 1,6 · 10 -4 (pKa s = 3,8). Fm 3+ muodostaa komplekseja erilaisten orgaanisten ligandien kanssa, joissa on kovia luovuttajaatomeja, kuten happea; ja nämä kompleksit ovat yleensä vakaampia kuin edeltävien aktinidien. Se muodostaa myös anionisia komplekseja ligandien kuten kloridin tai nitraatin kanssa; ja nämä kompleksit näyttävät myös olevan vakaampia kuin Einsteiniumin tai Californiumin kompleksit. Oletetaan, että korkeampien aktinidien komplekseissa olevalla sidoksella on enimmäkseen ioninen luonne: Fm 3+ -ioni on odotetusti pienempi kuin edelliset An 3+ -ionit - johtuen korkeammasta fermiumin tehokkaasta ydinsäiliöstä; ja sen myötä fermium muodostaisi todennäköisesti lyhyempiä ja vahvempia metalli-ligandisidoksia.
turvallisuusohjeet
CLP-asetuksen mukaisia luokituksia ei ole saatavilla, koska ne sisältävät vain kemiallisen vaaran ja niillä on täysin toissijainen asema verrattuna radioaktiivisuuteen liittyviin vaaroihin. Jälkimmäistä sovelletaan myös vain, jos kyseessä olevan aineen määrä on merkityksellinen.
käyttää
Fermium - yhdisteiden muodossa liuoksena - saadaan pääasiassa pieninä määrinä tutkimustarkoituksiin. Fermiumin yhdisteitä ei ole vielä esitetty kiinteässä muodossa.
kirjallisuus
- Robert J.Silva: Fermium , Mendelevium, Nobelium ja Lawrencium , julkaisussa: Lester R.Morss, Norman M.Edelstein, Jean Fuger (toim.): The Activity of Actinide and Transactinide Elements , Springer, Dordrecht 2006; ISBN 1-4020-3555-1 , s. 1621-1651 ( doi: 10.1007 / 1-4020-3598-5_13 ).
- Glenn T. Seaborg (Toim.): Elementtien 99 ja 100 25-vuotisjuhlaa muistavan symposiumin kokoukset , 23. tammikuuta 1978; Raportti LBL-7701, huhtikuu 1979.
- Gmelinin epäorgaanisen kemian käsikirja , järjestelmä nro 71, transuraani: osa A 1 II, s. 19-20; Osa A 2, s. 47; Osa B 1, s.84.
nettilinkit
- Merkintä fermiumiin. Julkaisussa: Römpp Online . Georg Thieme Verlag, käyty 3. tammikuuta 2015.
- Albert Ghiorso: Einsteinium ja Fermium , Chemical & Engineering News, 2003.
Yksittäiset todisteet
- ↑ Atomi- ja fysikaalisten ominaisuuksien (tietoruutu) arvot ovat peräisin: Robert J. Silva: Fermium, Mendelevium, Nobelium ja Lawrencium , julkaisussa: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Toim. ): Actinide and Transactinide Elements -kemia , Springer, Dordrecht 2006; ISBN 1-4020-3555-1 , s. 1621-1651.
- ↑ b c d e Merkintä fermium vuonna Kramida, A., Ralchenko, Yu., Reader, J. ja NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1) . Toim.: NIST , Gaithersburg, MD. doi : 10.18434 / T4W30F ( https://physics.nist.gov/asd ). Haettu 13. kesäkuuta 2020.
- ↑ a b c d e Entry on fermium at WebElements, https://www.webelements.com , käyty 13. kesäkuuta 2020.
- ↑ Radioaktiivisuuden aiheuttamat vaarat eivät kuulu ominaisuuksiin, jotka luokitellaan GHS-merkintöjen mukaan. Muiden vaarojen osalta tätä elementtiä ei ole vielä luokiteltu tai luotettavaa ja mainittavaa lähdettä ei ole vielä löydetty.
- B a b c d e f g h Albert Ghiorso: Einsteinium and Fermium , Chemical & Engineering News, 2003.
- ^ Albert Ghiorso , G.Bernard Rossi, Bernard G.Harvey, Stanley G.Thompson: U 238 : n reaktiot syklotronilla tuotettujen typpi-ionien kanssa , julkaisussa: Physical Review , 1954 , 93 (1), s. 257-257 ( doi: 10.1103 / PhysRev.93.257 ).
- ↑ SG Thompson, A. Ghiorso, BG Harvey, GR Choppin: Transcurium-isotoopit, jotka on tuotettu Plutoniumin neutronisäteilytyksessä , julkaisussa: Physical Review , 1954 , 93 (4), s.908-908 ( doi: 10.1103 / PhysRev.93.908 ) .
- ^ BG Harvey, SG Thompson, A. Ghiorso, GR Choppin: Transkuriuminuklidien lisätuotanto neutronisäteilytyksellä , julkaisussa: Physical Review , 1954 , 93 (5), s. 1129-1129 ( doi: 10.1103 / PhysRev.93.1129 ).
- ↑ MH Studier, PR-kentät, H. Diamond, JF Mech, AM Friedman, PA Sellers, G. Pyle, CM Stevens, LB Magnusson, JR Huizenga: Elements 99 and 100 from Pile-Irradiated Plutonium , julkaisussa: Physical Review , 1954 , 93 (6), s. 1428-1428 ( doi: 10.1103 / PhysRev.93.1428 ).
- ↑ PR Fields, MH Studier, JF Mech, H. Diamond, AM Friedman, LB Magnusson, JR Huizenga: Elementtien 99 ja 100 isotooppien lisäominaisuudet , julkaisussa: Physical Review , 1954 , 94 (1), s.209-210 ( doi: 10.1103 / PhysRev.94.209 ).
- ↑ GR Choppin, SG Thompson, A. Ghiorso, BG Harvey: Nuclear Properties of Some Isotopes of Californium, Elements 99 and 100 , julkaisussa: Physical Review , 1954 , 94 (4), s. 1080-1081 ( doi: 10.1103 / PhysRev .94,1080 ).
- ↑ Hugo Atterling, Wilhelm Forsling, Lennart W.Holm, Lars Melander, Björn Åström: Element 100 Produced by Means of Cyclotron-Accelerated Oxygen Ions , julkaisussa: Physical Review , 1954 , 95 (2), s.585-586 ( doi: 10.1103 / PhysRev.95.585.2 ).
- ^ A b G. T. Seaborg , SG Thompson, BG Harvey, GR Choppin: alkuaineiden 99 ja 100 kemialliset ominaisuudet ; Tiivistelmä ; Konekriptio (23. heinäkuuta 1954), Säteilylaboratorio, Kalifornian yliopisto, Berkeley, UCRL-2591 (Rev.) (PDF; 1,5 Mt).
- ^ A b S.G.Thompson, BG Harvey, GR Choppin, GT Seaborg: Elementtien 99 ja 100 kemialliset ominaisuudet , julkaisussa: J.Am. Chem. Soc. , 1954 , 76 (24), s. 6229-6236 ( doi: 10.1021 / ja01653a004 ).
- ^ A b A. Ghiorso, SG Thompson, GH Higgins, GT Seaborg ( Säteilylaboratorio ja kemian laitos, Kalifornian yliopisto, Berkeley, Kalifornia ), MH Studier, PR-kentät, SM Fried, H. Diamond, JF Mech, GL Pyle , JR Huizenga, A.Hirsch, WM Manning ( Argonnen kansallinen laboratorio, Lemont, Illinois ), CI Browne, HL Smith, RW Spence ( Los Alamosin tieteellinen laboratorio, Los Alamos, New Mexico ): New Elements Einsteinium and Fermium, Atomic Number 99 ja 100 , julkaisussa: Physical Review , 1955 , 99 (3), s. 1048-1049 ( doi: 10.1103 / PhysRev.99.1048 ; Maschinoscript (9. kesäkuuta 1955), Lawrence Berkeleyn kansallinen laboratorio. Paper UCRL-3036 ).
- ^ PR Fields, MH Studier, H. Diamond, JF Mech, MG Inghram, GL Pyle, CM Stevens, S. Fried, WM Manning ( Argonnen kansallinen laboratorio, Lemont, Illinois ); Ghiorso, SG Thompson, GH Higgins, GT Seaborg ( Kalifornian yliopisto, Berkeley, Kalifornia ): Transplutonium Elements in Thermonuclear Test Debris , julkaisussa: Physical Review , 1956 , 102 (1), s.180-182 ( doi: 10.1103) /PhysRev.102.180 ).
- ↑ David R. Lide: CRC Handbook of Chemistry and Physics , 85. painos, CRC Press, 2004, ISBN 978-0-8493-0485-9 , jakso 4, s. 4–10 ( rajoitettu esikatselu Google-teoshaulla). Tätä ei enää mainita 90. painoksessa (s. 4–12–4–13).
- ↑ G.Pfennig, H.Klewe-Nebenius, W.Seelmann-Eggebert (toim.): Karlsruher Nuklidkarte , 7. painos, 2006.
- ^ A b G.Audi, O.Bersillon, J.Blachot, AH Wapstra: NUBASE-arvio ydin- ja hajoamisominaisuuksista , julkaisussa: Nuclear Physics A , 729, 2003, s. 3–128. doi : 10.1016 / j.nuclphysa.2003.11.001 . ( PDF ; 1,0 Mt).
- B a b c d e f Robert J.Silva: Fermium , Mendelevium, Nobelium ja Lawrencium , julkaisussa: Lester R.Morss, Norman M.Edelstein, Jean Fuger (toim.): Actinide and Transactinide Elements , 3 3. painos, Springer, Dordrecht 2006, osa 3, s.1621-1651.
- ^ High Flux -isotooppireaktori , Oak Ridgen kansallinen laboratorio; Haettu 23. syyskuuta 2010.
- ↑ a b C.E.Porter, FD Riley, Jr., RD Vandergrift, LK Felker: Fermiumpuhdistus käyttäen Teva ™ -hartsiuutokromatografiaa , julkaisussa: syyskuu. Sci. Technol. , 1997 , 32 (1-4), s. 83-92 ( doi: 10.1080 / 01496399708003188 ).
- ↑ M. Sewtz, H. Backe, A. Dretzke, G. Kube, W. Lauth, P. Schwamb, K. Eberhardt, C. Grüning, P. Thörle, N. Trautmann, P. Kunz, J. Lassen, G Passler, CZ Dong, S. Fritzsche, RG Haire: Elementtifermiumin atomitasojen ensimmäinen havainto ( Z = 100) , julkaisussa: Phys. Tohtori Lett. , 2003 , 90 (16), s. 163002 ( doi: 10.1103 / PhysRevLett.90.163002 ).
- ^ RW Hoff, EK Hulet: Suunnittelu ydinräjähteillä , 1970 , 2 , s. 1283-1294.
- ^ GR Choppin, BG Harvey, SG Thompson: Uusi eluentti aktinidielementtien erottamiseksi , julkaisussa: J. Inorg. Nucl. Chem. , 1956 , 2 (1), s. 66-68 ( doi: 10.1016 / 0022-1902 (56) 80105-X ).
- ↑ NB Mikheev, AN Kamenskaya, NA Konovalova, IA Rumer, SA Kulyukhin: Nopea menetelmä fermiumin erottamiseksi aktinideista ja lantanideista , julkaisussa: Radiokhimiya , 1983 , 25 (2), s. 158-161.
- ↑ M.Jones, RP Schuman, JP Butler, G.Cowper, TA Eastwood, HG Jackson: Einsteiniumin ja Fermiumin isotoopit, tuotettu Plutonium Neutron Irradiation , julkaisussa: Physical Review , 1956 , 102 (1), s.203-207. ( doi: 10.1103 / PhysRev.102.203 ).
- ^ LI Guseva, KV Filippova, Yu. Gerlit, VA Druin, BF Myasoedov, NI Tarantin: Experiments on the production of Einsteinium and Fermium with a Cyclotron , julkaisussa: Journal of Nuclear Energy , 1954 , 3 (4), s. 341–346 (käännetty marraskuussa 1956) ( doi: 10.1016 / 0891-3919 (56) 90064-X ).
- ↑ NB Mikheev, VI Spitsyn, AN Kamenskaya, NA Konovalova, IA Rumer, LN Auerman, AM Podorozhnyi: Parin Fm 2+ / Fm 3+ hapetuspotentiaalin määrittäminen , julkaisussa: Inorg. Nucl. Chem. Lett. , 1977 , 13 (12), s. 651-656 ( doi: 10.1016 / 0020-1650 (77) 80074-3 ).
- ^ LJ Nugent, julkaisussa: MTP Int. Ilm. Sci.: Inorg. Chem., Ser. One , 1975 , 7 , s. 195-219.
- ↑ K. Samhoun, F. David, RL Hahn, GD O'Kelley, JR Tarrant, DE Hobart: Sähkökemiallinen tutkimus mendelevium vesiliuoksessa: ei näyttöä yksiarvoiset ionit , on: J. Inorg. Nucl. Chem. , 1979 , 41 (12), s. 1749-1754 ( doi: 10.1016 / 0022-1902 (79) 80117-7 ).
- ↑ Jaromír Malý: Raskaiden alkuaineiden yhdistämiskäyttäytyminen 1. Poikkeavan etusijan havaitseminen kaliforniumin, einsteiniumin ja fermiumin amalgaamien muodostumisessa julkaisussa: Inorg. Nucl. Chem. Lett. , 1967 , 3 (9), s. 373-381 ( doi: 10.1016 / 0020-1650 (67) 80046-1 ).
- ↑ NB Mikheev, VI Spitsyn, AN Kamenskaya, BA Gvozdec, VA Druin, IA Rumer, RA Dyachkova, NA Rozenkevitch, LN Auerman: Fermiumin pelkistyminen kaksiarvoiseen tilaan kloridin vesipitoisissa etanoliliuoksissa , julkaisussa: Inorg. Nucl. Chem. Lett. , 1972 , 8 (11), s. 929 - 936 ( doi: 10.1016 / 0020-1650 (72) 80202-2 ).
- ↑ EK Hulet, RW Lougheed, PA Baisden, JH Landrum, JF Wild, RF Lundqvist: Yksiarvoisen Md : n noudattamatta jättäminen , julkaisussa: J. Inorg. Nucl. Chem. , 1979 , 41 (12), s. 1743-1747 ( doi: 10.1016 / 0022-1902 (79) 80116-5 ).
- ^ Robert Lundqvist, EK Hulet, TA Baisden: Sähkömagneettinen menetelmä monimutkaisen kemian merkkiaineiden tutkimuksissa. II Kolmiarvoisten aktinidien hydratoidut säteet ja hydratointiluvut julkaisussa: Acta Chem. Scand., Ser. A , 1981 , 35 , s. 653-661 ( doi: 10,3891 / actachem.scand 35a-0653 ).
- ↑ H. Hussonnois, S. Hubert, L. Aubin, R. Guillaumont, G. Boussieres: Radiochem. Radioanal. Lett. , 1972 , 10 , s. 231 - 238.

![\ mathrm {^ {238} _ {\ 92} U \ {\ xrightarrow [{- 2 \ \ beta ^ {-}}] {+ \ 6 \ (n, \ gamma)}} \ _ {\ 94} ^ {244} Puh}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c4b60ac4bf0d4ebf96b6a71fefa86f13dd5784e0)
![\ mathrm {^ {238} _ {\ 92} U \ \ xrightarrow [-8 \ \ beta ^ -] {+ \ 15, \ 16, \ 17 \ (n, \ gamma)} \ ^ {253, \ 254 , \ 255} _ {\ \ \ \ \ \ \ \ \ \ \ \ \ 100} fm}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c2b40de4e6caa3766ff5f34a85f77466ab79326f)
![\ mathrm {^ {252} _ {\ 98} Cf \ {\ xrightarrow {(n, \ gamma)}} \ _ {\ 98} ^ {253} Cf \ {\ xrightarrow [{17.81 \ d}] {\ beta ^ {-}}} \ _ {\ 99} ^ {253} Se \ {\ xrightarrow {(n, \ gamma)}} \ _ {\ 99} ^ {254} It \ {\ xrightarrow [{}] {\ beta ^ {-}}} \ _ {100} ^ {254} Fm}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2dcf5875c42aad904ed8c8a397de8fc552cf5f71)


![\ mathrm {^ {257} _ {100} Fm \ \ xrightarrow [100.5 \ d] {\ alpha} \ ^ {253} _ {\ 98} Cf \ xrightarrow [17.81 \ d] {\ beta ^ -} \ ^ {253} _ {\ 99} Es \ xrightarrow [20.47 \ d] {\ alpha} \ ^ {249} _ {\ 97} Bk \ rightarrow \ ... \ rightarrow \ ^ {237} _ {\ 93 } Np}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0976bf22416778cd427bb5b7cf5b80a38f25162b)